Preliminary study on factors driving arbuscular mycorrhizal fungi diversity with elevation in the South-Tibet River Basin
-
摘要:
丛枝菌根真菌(Arbuscular mycorrhizal fungi,AMF)在维持高原湿地生态系统功能和促进其稳定性等方面发挥着重要作用,但AMF群落多样性及其构建过程对海拔的响应尚不清楚。本研究在藏南谷地沿4 200~5 100 m的海拔梯度进行了湿地植物调查、水体因子测定和土壤样品采集并分析。结果显示,藏南谷地湿地生态系统的AMF群落结构随海拔变异较大,其中以Glomus为优势属,且其相对丰度随海拔的上升呈显著下降的趋势。所有采样点中,AMF群落组成的差异以物种替换过程为主。变差分解结果表明,底泥和水体是解释AMF多样性海拔格局的主要环境因子。
Abstract:Arbuscular mycorrhizal fungi (AMF) play a vital role in maintaining the functionality and stability of plateau wetland ecosystems. However, the diversity of AMF communities along elevational gradients and their response to construction processes in the South-Tibet River Basin remain unclear. In this study, we conducted a wetland plant community survey, measured the physicochemical properties of water in situ, and collected sediment samples for further analysis across a high elevational gradient (4 200 to 5 100 m) in the South-Tibet River Basin. Results revealed that Glomus was the dominant genus within the Qinghai-Tibet Plateau wetland ecosystem. However, its relative abundance varied greatly with elevation, showing a significant declining trend with increasing elevation. Differences in AMF community composition were primarily due to species replacement. Variance partitioning analysis showed that the contribution of environmental variables to the AMF diversity-elevation patterns mainly involved sediment and water factors, with a lesser contribution from plant factors. These findings suggest that the establishment of the AMF community in the wetland habitat of the South-Tibet River Basin is predominantly governed by deterministic processes at high elevational gradients, reflecting a unique model of AMF community construction in the Qinghai-Tibet Plateau. However, further validation of these results is warranted.
-
丛枝菌根真菌(Arbuscular mycorrhizal fungi,AMF)是广泛存在于土壤中的微生物群,可以和大约80%的陆地植物根系形成共生结构[1]。AMF可以帮助植物根系吸收土壤中的营养元素(尤其是磷),作为回报,植物为AMF提供生长所必需的碳源,以此维持共生关系[2]。AMF与植物共生还能提高宿主植物应对非生物胁迫(如盐、旱和重金属等)的能力[3, 4]。然而,以往针对AMF群落结构的研究多集中在陆地生态系统中,有关湿地生态系统中AMF群落结构的报道较少。研究表明,湿地生境中底泥的低氧环境可能会抑制部分AMF的孢子萌发和生长,降低AMF的丰富度,进而影响湿地植物与AMF的共生[5]。然而,也有研究发现,部分湿地生境的底泥拥有较高的AMF丰富度,且AMF与湿地植物的共生对促进植物生长具有重要作用[6]。AMF与底泥中湿地植物根系共生关系的建立与后者拥有发达的通气组织有关,氧气经由通气组织扩散至根系,为AMF提供了必要的生存条件[7]。
AMF在维持湿地生态系统功能和稳定性方面具有重要意义。AMF和湿地植物的共生能提升湿地植物应对环境胁迫的能力,一定程度上可缓解湿地生态系统的退化,有助于维持湿地的生物多样性[8]。然而,当前AMF在高海拔湿地地区的分布特征和群落构建过程仍不清楚。尤其是在拥有独特地理位置的青藏高原地区,高海拔伴随着复杂的地形、温度和紫外辐射等条件,这些因素共同形成了强烈的生境过滤作用[9, 10]。在较短的地理距离范围内,湿地植物群落就能形成较大的差异,而AMF群落结构也可能在局域尺度上产生较大的差异。
青藏高原是我国重要的湿地分布区之一,拥有丰富的湿地资源,湿地面积达10.61×104 km2,占全国湿地面积的20%[11]。然而研究表明,青藏高原湿地正面临着不同程度的退化[12]。藏南谷地的海拔在3 500~5 500 m,属温带高原气候,湿地植物丰度较高[13],为研究湿地环境中AMF随海拔梯度的变化提供了自然的空间条件。在高海拔地区,较短的地理距离即可对气候和物种组成造成较大的差异。目前,沿海拔梯度对动植物多样性分布模式的研究已经较为广泛,但对微生物多样性的研究依然较少[14]。有研究表明,随着海拔的变化,微生物丰富度存在不同的变化趋势,包括随海拔呈单调递增、递减、单峰模式以及不显著等[15-17]。AMF作为湿地生态系统的重要组成部分,研究其在青藏高原湿地中的群落构建过程随海拔的变化趋势,将有助于更好地了解青藏高原湿地生态系统的功能和稳定性,为气候变化条件下青藏高原湿地的保护与修复提供科学依据。因此,本研究拟解决两个问题,一是在藏南谷地湿地环境中,随海拔梯度的变化,底泥中AMF群落结构存在什么样的差异; 二是AMF群落构建过程主要受什么因素的影响。
1. 材料与方法
1.1 研究区域概况
本研究于2021年7-8月在藏南谷地地区(27°97′~33°55′N,79°80′~89°64′E),沿4 200~5 100 m海拔梯度选取了20个样地进行采样(表1)。在每个样地选取3个2 m×2 m的湿地植物样方,用于调查湿地植物的种类。同时,在每个样方内采集1份底泥样品,最后将3个样方的底泥混合为1份不少于1 kg的底泥样品。底泥样品在湿地植物周围10 cm范围内采集。将底泥分为两部分,分别用于底泥理化因子以及AMF的分子测定。此外,在每个样地使用YSI Pro Plus多参数仪(Xylem,美国)现场测定水体指标,包括盐度(SAL),pH值,溶解氧(DO)和温度(T)。底泥样品采集后保存在4 ℃的车载冰箱中,最后运至实验室备用。
表 1 样地信息Table 1. Information on sampling sites样点
Sampling sites纬度
Latitude / N经度
Longitude / E海拔
Elevation / mSite 1 27°58′47″ 89°14′43″ 4 477 Site 2 28°12′42″ 88°47′35″ 4 732 Site 3 28°21′9″ 89°31′36″ 4 392 Site 4 28°55′7″ 87°25′55″ 5 059 Site 5 28°36′20″ 86°41′23″ 4 285 Site 6 28°36′37″ 86°43′35″ 4 281 Site 7 28°28′28″ 87°1′58″ 4 331 Site 8 28°44′36″ 86°9′21″ 4 465 Site 9 28°43′32″ 85°42′53″ 4 650 Site 10 29°53′6″ 84°23′51″ 5 022 Site 11 29°45′7″ 83°57′15″ 4 548 Site 12 29°51′57″ 83°44′29″ 4 553 Site 13 30°6′0″ 83°23′55″ 4 560 Site 14 30°37′25″ 82°13′54″ 4 780 Site 15 30°45′44″ 81°36′42″ 4 557 Site 16 31°8′24″ 80°54′37″ 4 581 Site 17 31°3′23″ 81°2′45″ 4 713 Site 18 32°2′36″ 80°5′32″ 4 271 Site 19 32°25′12″ 81°1′13″ 4 460 Site 20 32°56′12″ 79°48′7″ 4 343 1.2 土壤理化性质测定
将自然风干的底泥过100目筛后用于理化性质的测定,使用有机元素分析仪(Vario Macro Cube,德国)测定底泥中的总氮(TN) 和总碳(TC)含量。样品消煮后,使用电感耦合等离子体原子发射光谱仪(OPTIMA 8000DV,美国)测定总磷(TP)和总钾(TK)含量[18]。所有操作均在中国科学院武汉植物园公共实验室平台进行。
1.3 土壤DNA提取、PCR扩增及测序
将自然风干的底泥过100目筛后,用于AMF的分子测定,使用E.Z.N.A.土壤DNA试剂盒(Omega Biotek,Norcross,GA,美国),根据使用说明提取底泥总DNA,用Nano-Drop 2000 UV-vis分光光度计测定其浓度和纯度。PCR扩增时,对AMF功能基因高变区V4-V5区进行扩增,引物为AMV4-5N F(5′-AAGCTCGTAGTTGAATTTCG-3′)和 AMDG R(5′-CCCAACTATCCCTATTAATCAT-3′)。PCR重复 3次,从2%琼脂糖凝胶中回收扩增产物,利用AxyPrep DNA凝胶提取试剂盒(AxyPrep Biosciences,美国)进行纯化。
为了进行文库构建和PCR产物测序,首先采用Qubit 3.0方法对PCR产物进行定量,每24个不同条形码的扩增子均匀混合。按照Illumina制备基因组DNA文库的方法,将DNA构建配对端文库。使用Illumina MiSeq平台,按照标准方案对扩增子文库(2×250)进行配对测序。利用BLAST获得AMF的系统型,并将得到的序列(即操作分类单位,OTU)与MaarjAM数据库(http://maarjam.botany.ut.ee)[19]的基因序列进行比对。
1.4 统计分析
利用R程序包vegan,计算底泥中AMF的丰富度指数(Richness、Chao1指数和ACE指数)、多样性指数(Shannon指数和 Simpson指数)以及均匀度(Evenness指数)为代表的AMF群落α多样性指数,并计算植物群落多样性指数(Richness、Shannon指数以及invD指数)。
基于线性回归,分析海拔变化与底泥AMF的相关性。使用Mantel检验验证环境变量与AMF群落的显著性关系。使用变差分解(VPA)计算水体(DO、SAL、pH值和T)、植物(Richness、invD和Evenness指数)和底泥(TN、TP、TC和TK)3类变量对AMF群落的共同和独立贡献度[20]。在进行变差分解前,对AMF的OTU数据进行Hellinger转换,并用方差膨胀因子分析(VIF)去除具有多重共线性的变量(VIF<10)。
使用R程序包adespatial将各样点间的组成差异(β多样性)划分为替换(Replacement)和丰富度差异 (Richness difference),并分析β多样性对AMF群落组成变化的贡献度。为探究藏南谷地湿地环境中的AMF群落构建过程,先使用picante包,计算AMF的系统发育距离,再利用零模型方法计算βNTI值。当βNTI>2时,被认为显著高于预期的系统发育周转率,这被解释为确定性过程(Deterministic processes)的异质选择(Heterogeneous selection);当βNTI<−2时,则被认为是显著低于预期的系统发育周转率,这被解释为确定性过程的同质选择(Homogeneous selection);当βNTI 介于−2~2时,表明系统发育组成的差异是随机过程(Stochasticity processes)的结果。
上述分析均在R 4.1.3软件中完成。
2. 结果与分析
2.1 藏南谷地湿地中AMF群落随海拔的变化分析
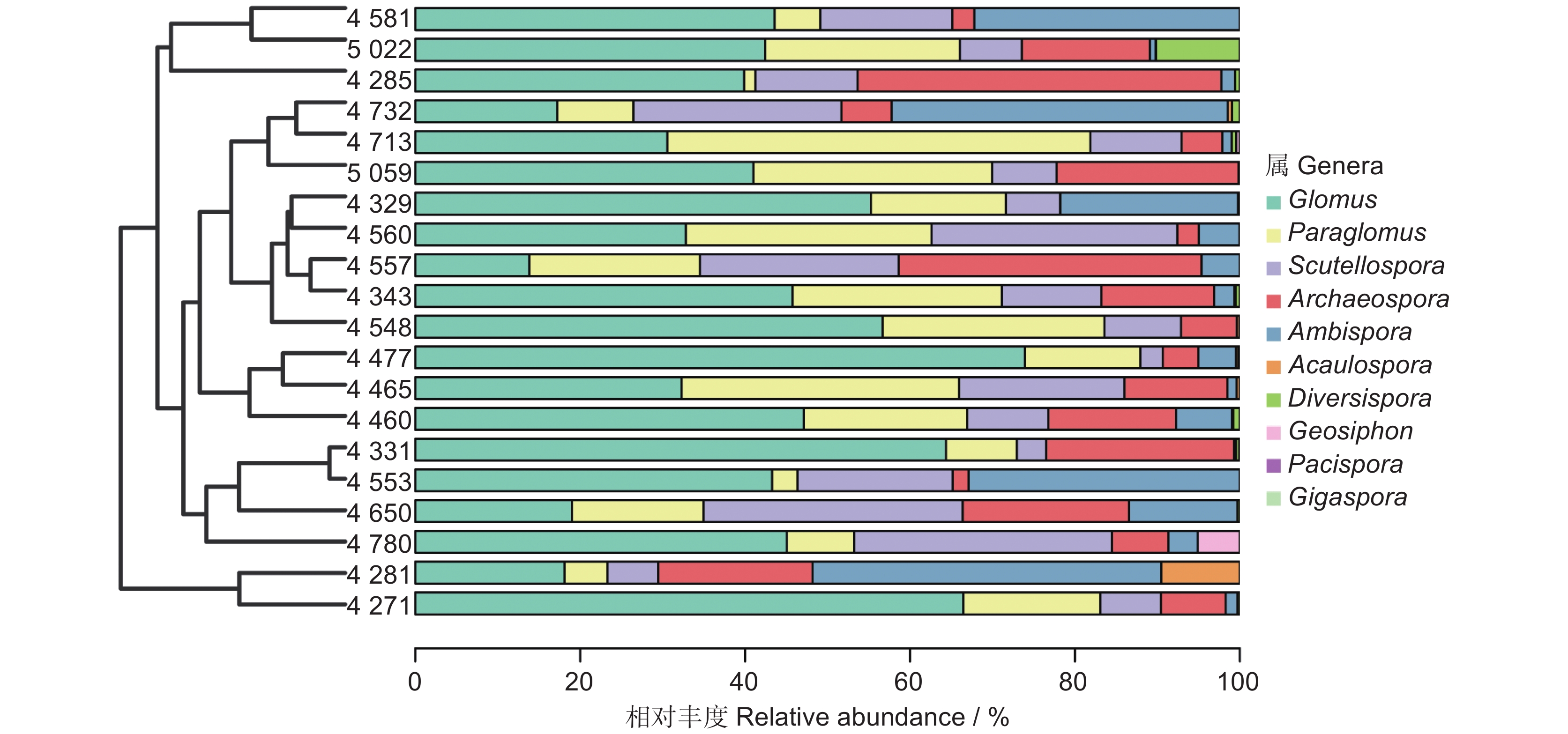
藏南谷地湿地环境中的AMF群落丰富度较高,共检测到130个OTUs,隶属于10个属(图1),其中丰度最高的属为Glomus(40.7%),其次是Paraglomus(17.5%)、Scutellospora (15.0%)、Archaeospora(13.6%)和Ambispora(11.8%),其余属的丰度均低于1%。
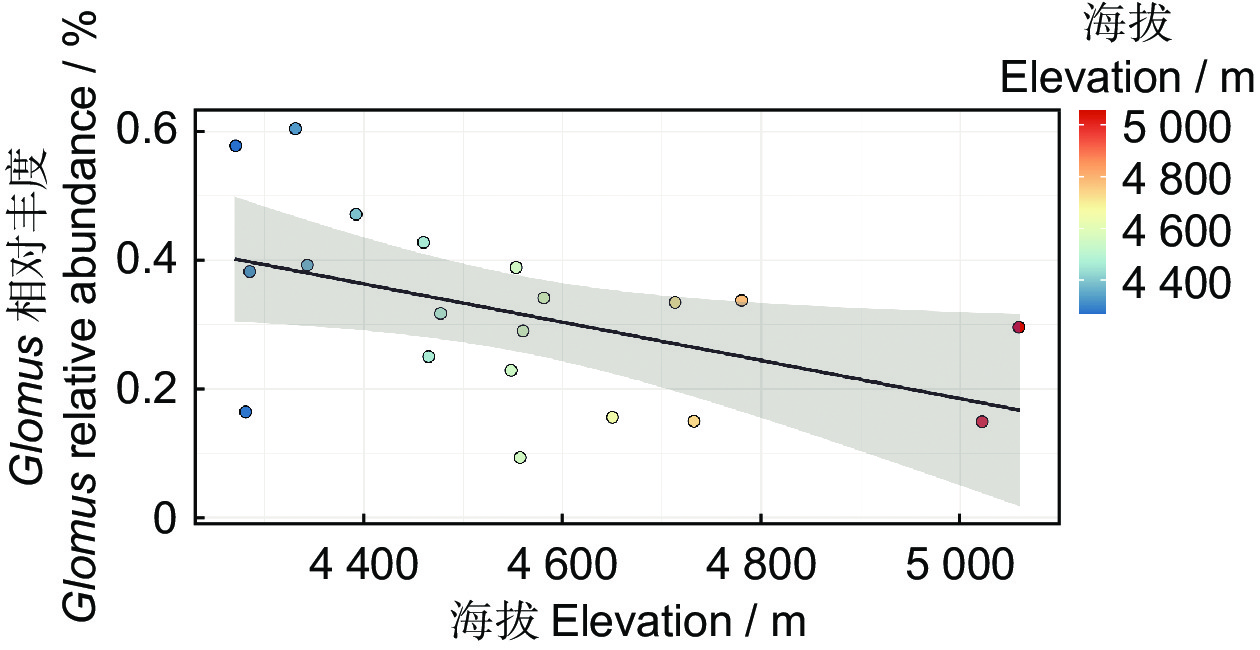
在藏南谷地湿地中,海拔梯度(4 200~5 100 m)与底泥AMF群落的相关性分析结果表明,优势属Glomus受海拔的影响较大,其相对丰度随海拔的上升呈显著下降的趋势(R2 =0.228,P<0.05)(图2)。部分稀有属在不同海拔上也有一定特异性的分布特征,如Geosiphon和Diversispora主要分布在较高海拔(4 780 m,Site 14)地区,而Acaulospora则主要分布在较低海拔(4 281 m,Site 6)地区。
2.2 AMF群落β多样性分析
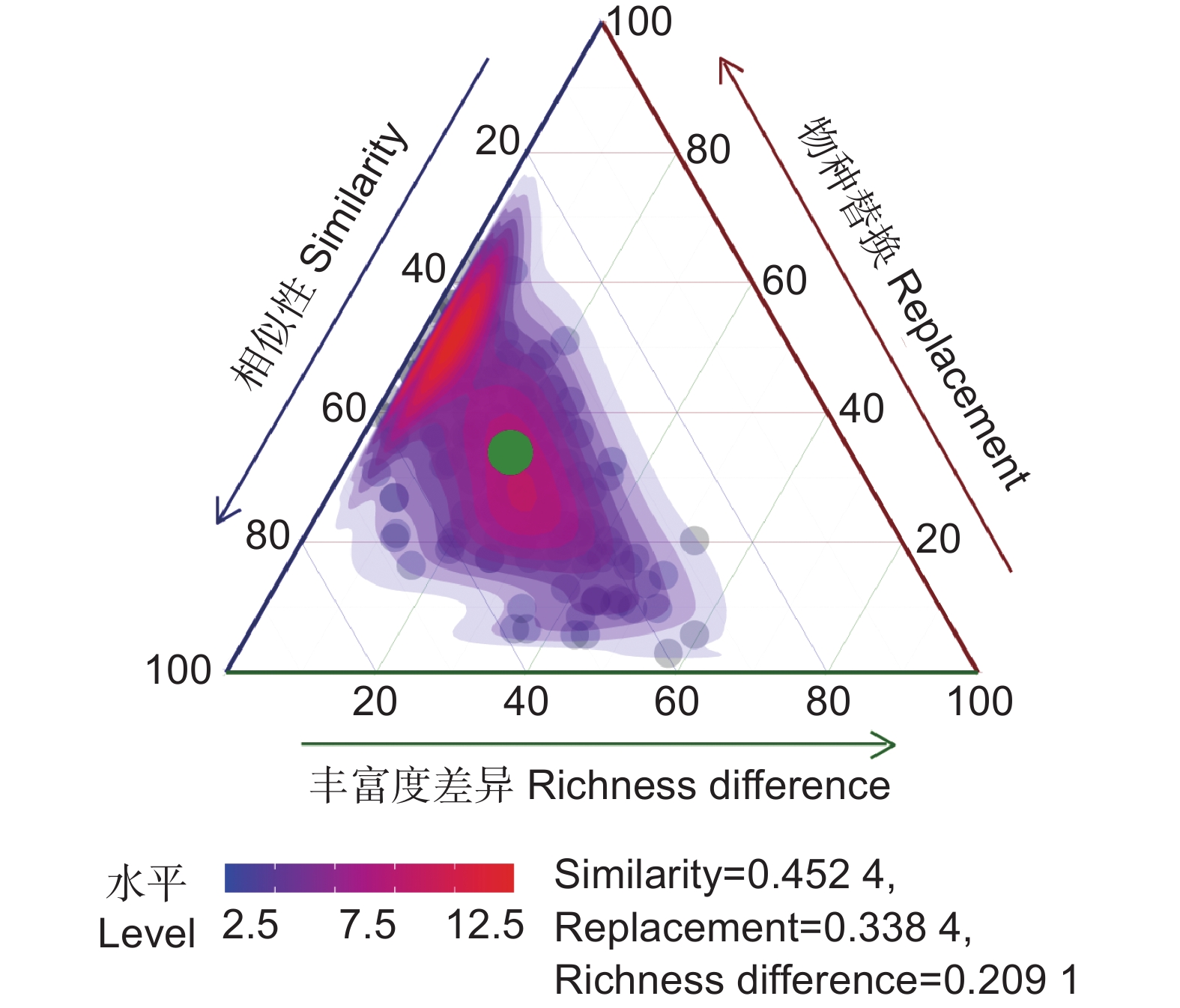
藏南谷地湿地环境中AMF真菌群落的β多样性分析结果表明,AMF群落组成在不同海拔(位点)间的差异以物种替换过程为主,其贡献度为61.8%;而丰富度差异过程对β多样性的贡献相对较小,仅占38.2%(图3)。
![]() 图 3 所有样点中AMF群落的β多样性比较三元图每个点代表一对样点,点的位置由相似性、物种替换和丰富度差异矩阵中的三元组值来共同确定,每个三元组的总和为1。Figure 3. Ternary map comparing β diversity of AMF communities at all sampling sitesEach point represents a pair of sampling points. Location of points was determined by triplet values of similarity, replacement, and richness difference matrix, with the sum of each triplet being 1.
图 3 所有样点中AMF群落的β多样性比较三元图每个点代表一对样点,点的位置由相似性、物种替换和丰富度差异矩阵中的三元组值来共同确定,每个三元组的总和为1。Figure 3. Ternary map comparing β diversity of AMF communities at all sampling sitesEach point represents a pair of sampling points. Location of points was determined by triplet values of similarity, replacement, and richness difference matrix, with the sum of each triplet being 1.2.3 藏南谷地湿地中AMF群落的构建过程
零模型分析结果显示,βNTI值主要集中在大于2的区间,表明在藏南谷地湿地中,确定性过程在AMF群落的构建中占主导地位。通过量化βNTI值,发现确定性过程占比大于随机性过程。确定性过程中只有变量选择,不存在同质选择;而随机性过程主要是由扩散限制(33.7%)和未主导过程(10%)组成,不存在同质扩散(表2)。
表 2 基于零模型分析的不同AMF群落构建过程的占比Table 2. Proportion of different AMF community assembly processes based on null model analysisAMF群落构建过程
AMF community assembly process样点
Sites
确定性异质选择 56.3% 同质选择 0
随机性扩散限制 33.7% 同质扩散 0 未主导过程 10.0% 2.4 不同环境变量对AMF群落结构差异的解释度
藏南谷地湿地中,对AMF群落结构差异的解释度可分为3部分,即底泥、水体和植物。水体指标包括DO、SAL、pH值以及T。本研究中,DO的值为1.32~11.72 mg/L,SAL为0.05‰~0.34‰,pH值在6.54~8.99,T值为8.5 ℃~24.9 ℃。底泥指标包括TC、TK、TP以及TN。TC为3.685~58.45 mg/g,TK为35.27~65.84 mg/g,TP为0.0165~0.6825 mg/g,TN为0.419~5.056 mg/g。本研究在藏南谷地湿样方中共发现32种湿地植物,隶属于19科28属,广泛分布于各个样点中的植物主要有三裂碱毛茛(Halerpestes tricuspis (Maxim.) Hand.-Mazz)、丝叶眼子菜(Stuckenia filiformis (Persoon) Borner)、海乳草(Lysimachia maritima (L.) Galasso, Banfi & Soldano)、西伯利亚蓼(Knorringia sibirica (Laxmann) Tzvelev)及水毛茛(Batrachium bungei (Steud.) L. Liou)等。基于底泥、水体和植物等环境因子开展AMF群落结构的变差分解分析,结果表明,底泥指标是影响AMF群落结构差异的主要因素,其贡献度为19.5%;其次是水体指标,贡献了15.2%的群落结构差异;植物的贡献度仅为7.9%(图4)。
利用Mantel检验单一环境因子与AMF群落的相关性,结果显示,AMF群落组成与水体pH值呈显著正相关(P<0.05),与水体温度也呈显著正相关(P<0.05)。此外,AMF群落还与植物群落的Evenness呈显著正相关(P<0.05)(表3)。
表 3 基于Mantel检验的环境因子对AMF群落的影响Table 3. Effects of environmental factors on AMF communities based on Mantel tests影响因素
Influencing factor相关系数
Correlation coefficientP值
P value总碳 0.036 0.289 总钾 −0.088 0.764 总磷 −0.129 0.894 溶解氧 0.088 0.286 盐度 0.044 0.354 pH值 0.247 0.041* 温度 0.220 0.048* 植物丰富度 0.033 0.358 植物invD指数 0.120 0.121 植物均匀度 0.245 0.031* 注:*表示相关性达到显著水平(P<0.05) 。 Note: * means significant difference at 0.05 level. 3. 讨论
3.1 藏南谷地湿地生态系统中AMF群落组成
本研究中,藏南谷地湿地环境底泥中AMF群落的优势属为Glomus(40.7%)和Paraglomus(17.5%),与前人报道一致[21]。Glomus对极端环境具有较强的适应能力和耐受能力,可以通过菌丝快速繁殖,并具有较高的孢子产生能力,因此,该属可以广泛存在于各种生境[22, 23]。同时,本研究发现,藏南谷地湿地底泥中AMF群落随海拔变化存在显著差异,Glomus的相对丰度随海拔上升呈下降趋势,与在青藏高原地区草原中进行的研究结果相一致[24],这表明海拔对AMF群落组成有较大的影响。Acaulospora在定日县的朋曲地区(海拔4 281 m,Site 6)有着较高的丰富度,而在海拔4 500 m以上则几乎没有发现,随海拔上升而呈下降趋势,与Gai等[25]在香格里拉(1 990~4 648 m)森林土壤中发现Acaulospor的丰富度在海拔4 648 m处达到最高,且随海拔上升而呈上升趋势的研究结果相反。这种变化规律的差异可能是因为,香格里拉地区的植物类群在高海拔地区由林下灌丛转变为高寒草甸,更有利于Acaulospor和草甸植物共生所导致。此外,本研究还发现,Geosiphon在4 500 m以下的低海拔地区丰富度较低,但在高海拔地区的普兰县公珠错(海拔4 780 m,Site 14)有着较高的丰富度。有研究指出,在高海拔地区温度较低,植物的生长季节比低海拔地区更短,这意味着在较高海拔地区植物分配给AMF的碳源同样也会减少,从而导致AMF在不同海拔地区存在差异[26]。本研究发现,部分AMF属(如Acaulospora)随着海拔的升高而逐渐消失,这可能是由于较高海拔(低温、高紫外线辐射等)的生境过滤,一些类群对恶劣环境更为敏感的结果[14]。该结果与AMF群落组成在不同海拔梯度上的差异以物种替换过程为主是相符的。
3.2 藏南谷地湿地中AMF群落构建
Fan等[27]的研究显示,青藏高原草地中,在AMF群落构建中起主导作用的是随机性过程。与该报道不同,本研究结果表明,藏南谷地湿地环境中,AMF群落构建过程主要是由确定性过程主导。其原因可能是藏南谷地湿地环境中AMF的扩散限制不同于青藏高原的草原地区。在草原地区,放牧等各种干扰更加频繁,而AMF孢子可以通过动物粪便和动物对土壤的扰动来促进AMF的扩散[28];此外放牧还会造成草原地区的生境破碎,进而影响AMF的群落构建过程[29]。藏南谷地湿地环境中,水体中较高的pH值以及底泥中较低的溶氧等生境过滤则可能影响AMF的群落构建。此外,AMF的群落构建在一定程度上取决于生境条件[30]。如,在荒漠化地区,AMF孢子的扩散通常依赖风力[31],而在林下环境中,土壤动物可以成为AMF的扩散动力[28]。不同土壤环境中的氮磷含量以及pH值差异同样也会影响AMF的群落构建[32]。藏南谷地湿地与荒漠、草原、林下相比,其环境的扰动相对较小,更有可能受水体pH值和底泥营养元素的限制,从而影响AMF群落构建。
3.3 藏南谷地湿地中不同变量对AMF群落的影响
本研究所关注的环境因子对AMF群落变异的解释度较低,尚有超过70%未能解释的方差变异。除了底泥、水体以及植物外,气候条件和植物种类等也是影响AMF群落结构的重要因素[33, 34]。如,一项对全世界327个土壤样品中AMF群落结构的整合分析研究结果表明,在众多环境变量中,气候变量(年降水量和年均温)是解释度最高的影响因素[35]。相比于水体和植物,底泥对 AMF 群落的单独解释度最高,达到19.5%,这与Sepp等[36]报道的底泥营养显著影响AMF群落相一致。也有研究认为,AMF能够帮助植物有效地吸收土壤氮磷元素[37]。而本研究中,总氮与底泥中AMF优势属Glomus的相对丰度具有显著相关性,随着总氮含量的上升,其相对丰度呈显著上升趋势。也有研究认为,底泥中的低溶氧环境可以直接影响AMF群落的生存能力,从而改变群落结构[38]。在阿根廷沿海湿地的研究表明,螃蟹洞穴显著增加了底泥中的溶氧,从而提高了AMF的多样性以及湿地植物根系的定殖率[39]。另外,我们的结果显示,水体对AMF群落的独立解释度为15.2%。有研究表明,水体pH值可以间接影响底泥中养分的可用性,从而对AMF群落产生影响[40]。如,一项针对北京郊区湿地中AMF多样性的研究显示,芦苇(Phragmites australis (Cav.) Trin. ex Steud)根系的AMF定殖率与水体pH值显著相关[41]。本研究还发现,植物群落对AMF群落的贡献度并不高,这可能是由于本研究只选取了植物群落的α多样性进行分析,而并未深入研究植物群落的根系结构特征。有报道指出,植物的根系结构会显著影响AMF的定殖,根毛密度较低的植物对AMF的依赖程度较高[42, 43]。此外,还可能与底泥样品的采集有关,有研究表明,根系分泌物可以直接影响根际微生物的组成[44]。本研究采集的底泥样品均为非根际土,这可能降低了植物对底泥中AMF群落差异的贡献度。
综上所述,本研究揭示了藏南谷地湿地环境中AMF群落结构随海拔变化的分布模式,发现AMF群落组成在不同海拔上的差异主要以物种替换过程为主,确定性过程主导了AMF的群落构建。此外,解释AMF群落结构变异最重要的因素是底泥,这可能和藏南谷地湿地中磷元素限制有关。但本研究调查的位点数较少,未来还需开展更大尺度的研究来验证上述结论。
-
图 3 所有样点中AMF群落的β多样性比较三元图
每个点代表一对样点,点的位置由相似性、物种替换和丰富度差异矩阵中的三元组值来共同确定,每个三元组的总和为1。
Figure 3. Ternary map comparing β diversity of AMF communities at all sampling sites
Each point represents a pair of sampling points. Location of points was determined by triplet values of similarity, replacement, and richness difference matrix, with the sum of each triplet being 1.
表 1 样地信息
Table 1 Information on sampling sites
样点
Sampling sites纬度
Latitude / N经度
Longitude / E海拔
Elevation / mSite 1 27°58′47″ 89°14′43″ 4 477 Site 2 28°12′42″ 88°47′35″ 4 732 Site 3 28°21′9″ 89°31′36″ 4 392 Site 4 28°55′7″ 87°25′55″ 5 059 Site 5 28°36′20″ 86°41′23″ 4 285 Site 6 28°36′37″ 86°43′35″ 4 281 Site 7 28°28′28″ 87°1′58″ 4 331 Site 8 28°44′36″ 86°9′21″ 4 465 Site 9 28°43′32″ 85°42′53″ 4 650 Site 10 29°53′6″ 84°23′51″ 5 022 Site 11 29°45′7″ 83°57′15″ 4 548 Site 12 29°51′57″ 83°44′29″ 4 553 Site 13 30°6′0″ 83°23′55″ 4 560 Site 14 30°37′25″ 82°13′54″ 4 780 Site 15 30°45′44″ 81°36′42″ 4 557 Site 16 31°8′24″ 80°54′37″ 4 581 Site 17 31°3′23″ 81°2′45″ 4 713 Site 18 32°2′36″ 80°5′32″ 4 271 Site 19 32°25′12″ 81°1′13″ 4 460 Site 20 32°56′12″ 79°48′7″ 4 343 表 2 基于零模型分析的不同AMF群落构建过程的占比
Table 2 Proportion of different AMF community assembly processes based on null model analysis
AMF群落构建过程
AMF community assembly process样点
Sites
确定性异质选择 56.3% 同质选择 0
随机性扩散限制 33.7% 同质扩散 0 未主导过程 10.0% 表 3 基于Mantel检验的环境因子对AMF群落的影响
Table 3 Effects of environmental factors on AMF communities based on Mantel tests
影响因素
Influencing factor相关系数
Correlation coefficientP值
P value总碳 0.036 0.289 总钾 −0.088 0.764 总磷 −0.129 0.894 溶解氧 0.088 0.286 盐度 0.044 0.354 pH值 0.247 0.041* 温度 0.220 0.048* 植物丰富度 0.033 0.358 植物invD指数 0.120 0.121 植物均匀度 0.245 0.031* 注:*表示相关性达到显著水平(P<0.05) 。 Note: * means significant difference at 0.05 level. -
[1] Wang B,Qiu YL. Phylogenetic distribution and evolution of mycorrhizas in land plants[J]. Mycorrhiza,2006,16(5):299−363. doi: 10.1007/s00572-005-0033-6
[2] Wang GW,Jin ZX,George TS,Feng G,Zhang L. Arbuscular mycorrhizal fungi enhance plant phosphorus uptake through stimulating hyphosphere soil microbiome functional profiles for phosphorus turnover[J]. New Phytol,2023,238(6):2578−2593. doi: 10.1111/nph.18772
[3] Li MH,Cai P,Hou SW,Cheng Z,Wu FY,et al. Degradation of soil arbuscular mycorrhizal fungal diversity and functionality accompanied by the aggravation of pepper Phytophthora blight in a facility shed in Southwest China[J]. Land Degrad Dev,2022,33(9):1337−1346. doi: 10.1002/ldr.4228
[4] Grünfeld L,Skias G,Rillig MC,Veresoglou SD. Arbuscular mycorrhizal root colonization depends on the spatial distribution of the host plants[J]. Mycorrhiza,2022,32(5-6):387−395. doi: 10.1007/s00572-022-01087-0
[5] Huang GM,Srivastava AK,Zou YN,Wu QS,Kuča K. Exploring arbuscular mycorrhizal symbiosis in wetland plants with a focus on human impacts[J]. Symbiosis,2021,84(3):311−320. doi: 10.1007/s13199-021-00770-8
[6] Andersen FØ,Andersen T. Effects of arbuscular mycorrhizae on biomass and nutrients in the aquatic plant Littorella uniflora[J]. Freshwater Biol,2006,51(9):1623−1633. doi: 10.1111/j.1365-2427.2006.01608.x
[7] Xu ZY,Ban YH,Jiang YH,Zhang XL,Liu XY. Arbuscular mycorrhizal fungi in wetland habitats and their application in constructed wetland:a review[J]. Pedosphere,2016,26(5):592−617. doi: 10.1016/S1002-0160(15)60067-4
[8] 吴松,隋心,张童,陈雨彤,朱道光,等. 湿地丛枝菌根真菌研究进展[J]. 国土与自然资源研究,2019(6):80−84. Wu S,Sui X,Zhang T,Chen YT,Zhu DG,et al. Research on the progress of AMF in wetland[J]. Territory & Natural Resources Study,2019(6):80−84.
[9] Dolezal J,Dvorsky M,Kopecky M,Liancourt P,Hiiesalu I,et al. Vegetation dynamics at the upper elevational limit of vascular plants in Himalaya[J]. Sci Rep,2016,6:24881. doi: 10.1038/srep24881
[10] Zhang B,Xue K,Zhou ST,Che RX,Du JQ,et al. Phosphorus mediates soil prokaryote distribution pattern along a small-scale elevation gradient in Noijin Kangsang Peak,Tibetan Plateau[J]. FEMS Microbiol Ecol,2019,95(6):fiz076. doi: 10.1093/femsec/fiz076
[11] 张倚浩,阎建忠,程先. 气候变化与人类活动对青藏高原湿地的影响研究进展[J]. 生态学报,2023,43(6):2180−2193. Zhang YH,Yan JZ,Cheng X. Advances in impact of climate change and human activities on wetlands on the Tibetan Plateau[J]. Acta Ecologica Sinica,2023,43(6):2180−2193.
[12] 赵魁义,王德斌,宋海远. 西藏高原沼泽的初步研究[J]. 自然资源,1981(2):14−21. [13] Wang N,Gao J,Zhang SQ,Wang GX. Variations in leaf and root stoichiometry of Nitraria tangutorum along aridity gradients in the Hexi Corridor,Northwest China[J]. Contemp Probl Ecol,2014,7(3):308−314. doi: 10.1134/S1995425514030123
[14] Liu L,Hart MM,Zhang JL,Cai XB,Gai JP,et al. Altitudinal distribution patterns of AM fungal assemblages in a Tibetan alpine grassland[J]. FEMS Microbiol Ecol,2015,91(7):fiv078. doi: 10.1093/femsec/fiv078
[15] Fierer N,McCain CM,Meir P,Zimmermann M,Rapp JM,et al. Microbes do not follow the elevational diversity patterns of plants and animals[J]. Ecology,2011,92(4):797−804. doi: 10.1890/10-1170.1
[16] Singh D,Takahashi K,Adams JM. Elevational patterns in archaeal diversity on Mt. Fuji[J]. PLoS One,2012,7(9):e44494. doi: 10.1371/journal.pone.0044494
[17] Bryant JA,Lamanna C,Morlon H,Kerkhoff AJ,Enquist BJ,Green JL. Microbes on mountainsides:contrasting elevational patterns of bacterial and plant diversity[J]. Proc Natl Acad Sci USA,2008,105(S1):11505−11511.
[18] Hou EQ,Luo YQ,Kuang YW,Chen CR,Lu XK,et al. Global meta-analysis shows pervasive phosphorus limitation of aboveground plant production in natural terrestrial ecosystems[J]. Nat Commun,2020,11(1):637. doi: 10.1038/s41467-020-14492-w
[19] Öpik M,Vanatoa A,Vanatoa E,Moora M,Davison J,et al. The online database MaarjAM reveals global and ecosystemic distribution patterns in arbuscular mycorrhizal fungi (Glomeromycota)[J]. New Phytol,2010,188(1):223−241. doi: 10.1111/j.1469-8137.2010.03334.x
[20] Yang T,Adams JM,Shi Y,He JS,Jing X,et al. Soil fungal diversity in natural grasslands of the Tibetan Plateau:associations with plant diversity and productivity[J]. New Phytol,2017,215(2):756−765. doi: 10.1111/nph.14606
[21] Hart MM,Reader RJ. Taxonomic basis for variation in the colonization strategy of arbuscular mycorrhizal fungi[J]. New Phytol,2002,153(2):335−344. doi: 10.1046/j.0028-646X.2001.00312.x
[22] Daniell TJ,Husband R,Fitter AH,Young JPW. Molecular diversity of arbuscular mycorrhizal fungi colonising arable crops[J]. FEMS Microbiol Ecol,2001,36(2-3):203−209. doi: 10.1111/j.1574-6941.2001.tb00841.x
[23] Ouyang JX,He YD,Yang B,Zhou JZ,Li W,Cao Y. Elevation,but not phosphorus,shapes arbuscular mycorrhizal fungal colonization of plateau wetland plants:a case study of the Qinghai-Tibet Plateau[J]. Glob Ecol Conserv,2023,46:e02611.
[24] Li XL,Gai JP,Cai XB,Li XL,Christie P,et al. Molecular diversity of arbuscular mycorrhizal fungi associated with two co-occurring perennial plant species on a Tibetan altitudinal gradient[J]. Mycorrhiza,2014,24(2):95−107. doi: 10.1007/s00572-013-0518-7
[25] Gai JP,Tian H,Yang FY,Christie P,Li XL,Klironomos JN. Arbuscular mycorrhizal fungal diversity along a Tibetan elevation gradient[J]. Pedobiologia,2012,55(3):145−151. doi: 10.1016/j.pedobi.2011.12.004
[26] Antoninka A,Reich PB,Johnson NC. Seven years of carbon dioxide enrichment,nitrogen fertilization and plant diversity influence arbuscular mycorrhizal fungi in a grassland ecosystem[J]. New Phytol,2011,192(1):200−214. doi: 10.1111/j.1469-8137.2011.03776.x
[27] Fan DD,Ji MK,Wu JS,Chen H,Jia HZ,et al. Grazing does not influence soil arbuscular mycorrhizal fungal diversity,but increases their interaction complexity with plants in dry grasslands on the Tibetan Plateau[J]. Ecol Indic,2023,148:110065. doi: 10.1016/j.ecolind.2023.110065
[28] Vályi K,Mardhiah U,Rillig MC,Hempel S. Community assembly and coexistence in communities of arbuscular mycorrhizal fungi[J]. ISME J,2016,10(10):2341−2351. doi: 10.1038/ismej.2016.46
[29] Shi GX,Yao BQ,Liu YJ,Jiang SJ,Wang WY,et al. The phylogenetic structure of AMF communities shifts in response to gradient warming with and without winter grazing on the Qinghai-Tibet Plateau[J]. Appl Soil Ecol,2017,121:31−40. doi: 10.1016/j.apsoil.2017.09.010
[30] Cheng YK,Liu X,Lu YW,Chen F,Zhou XH,et al. Long-term nitrogen fertilization alters phylogenetic structure of arbuscular mycorrhizal fungal community in plant roots across fine spatial scales[J]. Plant Soil,2023,483(1-2):427−440. doi: 10.1007/s11104-022-05753-2
[31] Egan C,Li DW,Klironomos J. Detection of arbuscular mycorrhizal fungal spores in the air across different biomes and ecoregions[J]. Fungal Ecol,2014,12:26−31. doi: 10.1016/j.funeco.2014.06.004
[32] Johnson NC. Resource stoichiometry elucidates the structure and function of arbuscular mycorrhizas across scales[J]. New Phytol,2010,185(3):631−647. doi: 10.1111/j.1469-8137.2009.03110.x
[33] Řezáčová V,Slavíková R,Konvalinková T,Zemková L,Řezáč M,et al. Geography and habitat predominate over climate influences on arbuscular mycorrhizal fungal communities of mid-European meadows[J]. Mycorrhiza,2019,29(6):567−579. doi: 10.1007/s00572-019-00921-2
[34] Lin GG,McCormack ML,Guo DL. Arbuscular mycorrhizal fungal effects on plant competition and community structure[J]. J Ecol,2015,103(5):1224−1232. doi: 10.1111/1365-2745.12429
[35] Davison J,Moora M,Semchenko M,Adenan SB,Ahmed T,et al. Temperature and pH define the realised niche space of arbuscular mycorrhizal fungi[J]. New Phytol,2021,231(2):763−776. doi: 10.1111/nph.17240
[36] Sepp SK,Davison J,Jairus T,Vasar M,Moora M,et al. Non-random association patterns in a plant-mycorrhizal fungal network reveal host-symbiont specificity[J]. Mol Ecol,2019,28(2):365−378. doi: 10.1111/mec.14924
[37] Hodge A,Fitter AH. Substantial nitrogen acquisition by arbuscular mycorrhizal fungi from organic material has implications for N cycling[J]. Proc Natl Acad Sci USA,2010,107(31):13754−13759. doi: 10.1073/pnas.1005874107
[38] Wolfe BE,Mummey DL,Rillig MC,Klironomos JN. Small-scale spatial heterogeneity of arbuscular mycorrhizal fungal abundance and community composition in a wetland plant community[J]. Mycorrhiza,2007,17(3):175−183. doi: 10.1007/s00572-006-0089-y
[39] Daleo P,Fanjul E,Casariego AM,Silliman BR,Bertness MD,Iribarne O. Ecosystem engineers activate mycorrhizal mutualism in salt marshes[J]. Ecol Lett,2007,10(10):902−908. doi: 10.1111/j.1461-0248.2007.01082.x
[40] Ren LJ,Jeppesen E,He D,Wang JJ,Liboriussen L,et al. pH influences the importance of niche-related and neutral processes in lacustrine bacterioplankton assembly[J]. Appl Environ Microbiol,2015,81(9):3104−3114. doi: 10.1128/AEM.04042-14
[41] Wang SG,Dai DW,Song S,Diao XJ,Ma LM. Arbuscular mycorrhizal (AM) status in urban wetland plants and its impact factors[J]. Aquat Bot,2018,150:33−45. doi: 10.1016/j.aquabot.2018.07.002
[42] Muthukumar T,Udaiyan K,Shanmughavel P. Mycorrhiza in sedges:an overview[J]. Mycorrhiza,2004,14(2):65−77. doi: 10.1007/s00572-004-0296-3
[43] Orfanoudakis M,Wheeler CT,Hooker JE. Both the arbuscular mycorrhizal fungus Gigaspora rosea and Frankia increase root system branching and reduce root hair frequency in Alnus glutinosa[J]. Mycorrhiza,2010,20(2):117−126. doi: 10.1007/s00572-009-0271-0
[44] Mommer L,Kirkegaard J,van Ruijven J. Root-root interactions:towards a rhizosphere framework[J]. Trends Plant Sci,2016,31(3):209−217.
-
期刊类型引用(1)
1. 苗婷婷,吴中能,刘俊龙,王新,王继承,曹志华,孙慧. 不同薄壳山核桃品种(系)对自然干旱胁迫的生理响应及抗旱性评价. 安徽林业科技. 2025(01): 14-22+34 .  百度学术
百度学术
其他类型引用(0)



 下载:
下载: