Metabolite changes in new shoots of Camellia sinensis (L.) O. Kuntze infested by tea aphids
-
摘要:
茶蚜是春季茶树(Camellia sinensis (L.) O. Kuntze)的主要害虫,严重影响茶叶的产量和品质。次生代谢物质在植物防御蚜虫危害过程中具有重要作用,研究茶蚜为害下茶树新梢次生代谢物的变化有利于筛选和培育抗蚜茶树品种。本研究以茶蚜为害和未为害的茶树品种‘鄂茶一号’新梢为材料,开展了代谢组学分析和主要代谢物定量分析,检测了苯丙氨酸解氨酶(PAL)、多酚氧化酶(PPO)活性和脯氨酸(Pro)含量。结果显示,‘鄂茶一号’茶蚜危害率高达35.4%,对茶蚜中等抗性。茶蚜为害后,新梢中PAL活性轻微上升,PPO活性显著提高,可溶性糖、黄酮和Pro含量显著上升,而茶多酚含量显著下降。茶蚜为害诱导了8个代谢物质显著差异变化,包括3个初生代谢物和5个次生代谢物。3个初生代谢物全部上调表达,可能为次生代谢物合成提供前体,也可能改变茶蚜生存所需的营养物质。5个次生代谢物包括1个茉莉酸类物质JA-Ile和4个类黄酮物质,JA-Ile作为防御信号物质显著上调表达,激活茶树下游防御体系,类黄酮作为防御物质直接参与茶蚜防御。研究结果表明JA-Ile、类黄酮和Pro可能是茶树防御茶蚜的主要物质。
Abstract:Tea aphids are a major insect pest of tea plants (Camellia sinensis (L.) O. Kuntze), resulting in both tea production loss and tea quality decline. Secondary metabolites play vital roles in plant resistance against aphid feeding. Therefore, understanding changes in metabolites before and after tea aphid infestation is essential for the screening and breeding of aphid-resistant tea varieties. In the current study, metabolomics profiling, quantitative analysis of metabolites, and determination of phenylalanine ammonia-lyase (PAL) and polyphenol oxidase (PPO) activities and proline (Pro) content were performed in new shoots of the ‘Echa 1’ tea variety infested with tea aphids, using non-infested plants as controls. Results showed that 35.4% of ‘Echa 1’ was colonized by tea aphids, suggesting that ‘Echa 1’ exhibited medium resistance to tea aphids. In parallel, significantly higher PPO activity, markedly higher soluble sugar, total flavonoid, and Pro contents, and significantly lower tea polyphenol content were found after aphid infestation. Eight significantly accumulated metabolites, including three primary metabolites and five secondary metabolites, were also detected. The three primary metabolites were all up-regulated in aphid-impacted shoots, which may confer precursors for secondary metabolite biosynthesis and modify the nutritional compounds utilized by tea aphids. The five secondary metabolites included jasmonate-isoleucine (JA-Ile) and four flavonoids. JA-Ile, responsible for defense-related signaling molecules, was significantly up-regulated after aphid-feeding, functioning in the activation of downstream defensive pathways, while the flavonoids served as defense compounds against the tea aphids. Taken together, these results suggest that JA-Ile, flavonoids, and Pro are important defensive compounds against tea aphids in tea plants.
-
Keywords:
- Camellia sinensis cv. ‘Echa 1’ /
- New shoots /
- Tea aphids /
- Metabolites /
- Defense
-
茶树(Camellia sinensis (L.) O. Kuntze)是我国重要的叶用特色经济作物,以茶树芽、叶加工而成的茶叶是我国传统的特色优势产业,也是茶区乡村振兴的支柱产业。茶蚜是春季茶树的主要害虫,常成群聚集新梢危害,严重时新梢芽叶卷曲变黄,茶叶产量下降、品质降低。目前,茶蚜防治主要依靠喷施农药,不仅增加劳动力和经济成本,且可造成农药残留,威胁生态环境和茶叶质量安全。因此,了解茶树对茶蚜的防御响应,培育茶蚜抗性茶树品种才是防治茶蚜危害的有效方法。
蚜虫通过取食植物韧皮部汁液获取营养,汁液中营养物质和防御物质的组成和水平影响蚜虫的取食和繁殖行为[1, 2]。研究发现,植物营养物质中的可溶性糖和氨基酸为蚜虫提供所需的碳源和氮源,是蚜虫生存的主要限制因子[1-4];植物次生代谢物质如生物碱、有机酸、类黄酮、酚酸类和萜类等是主要的防御物质,参与植物防御蚜虫危害[1, 3, 5-7]。相反,蚜虫取食也会诱导植物营养物质和次生代谢物水平的变化[1, 2, 8]。
植物遭受蚜虫取食时,首先通过感知激活防御相关信号分子途径。蚜虫防御相关的信号分子包括激素信号分子如茉莉酸(JA)及其衍生物、水杨酸(SA)和乙烯,及活性氧(ROS)/活性氮(RNS)信号分子如过氧化氢和一氧化氮[1, 9-11]。研究表明,JA和SA是主要的蚜虫防御信号分子,二者单独或者拮抗/协同发挥调控作用[3, 9]。信号分子的级联传递,将触发下游防御基因及防御蛋白差异表达,最终植物通过调控自身营养物质水平及次生代谢物含量等进行自我防御[3, 5-7, 12, 13]。苯丙氨酸解氨酶(PAL)和多酚氧化酶(PPO)是植物次生代谢物合成途径上的关键酶类,现已证实是植物防御蚜虫的主要酶类[14-17]。
茶树新梢富含各种营养物质和茶多酚、生物碱、类黄酮等多种次生代谢物。在蚜虫取食时,新梢中的营养物质和次生代谢物的变化却甚少报道。近期,冉伟[5]开展了‘龙井43’叶片接种茶蚜2 d和6 d后代谢物的变化研究,结果表明茶蚜为害2 d和6 d均引起了叶片代谢物质的重新分配,差异化合物主要参与碳水化合物、氨基酸和有机酸的合成与代谢。然而,在茶蚜为害的‘龙井43’叶片中茶多酚、生物碱、类黄酮等主要次生代谢物的变化却鲜有提及。为了全面解析茶蚜取食后茶树代谢物的变化,本研究以茶蚜未为害和为害的茶树品种‘鄂茶一号’新梢为试材,采用广泛靶向代谢组学技术和主要代谢物质定量分析技术,鉴定响应茶蚜的重要次生代谢物,以期为茶蚜防控及抗蚜茶树品种培育提供指导。
1. 材料与方法
1.1 植物材料
以湖北省茶树种质资源圃‘鄂茶一号’15年茶树为供试材料。于2022年3月30日,在试验小区内选定调查框,采集框内新梢用于研究茶蚜危害情况。同时,在小区内采集茶蚜未为害的‘鄂茶一号’一芽二叶和一芽三叶各20个,混合后设置为茶蚜未为害(‘Echa 1’ uninfested by aphid,EN)组;采集茶蚜为害的一芽二叶和一芽三叶各20个,混合后设置为茶蚜为害(‘Echa 1’ infested by aphid,EA)组。EN和EA组各重复3次,液氮速冻后保存于−80 ℃用于后续研究。
1.2 方法
1.2.1 茶蚜危害和分布分析
在 ‘鄂茶一号’试验小区的采摘面(13.5 m2)上,采用平行跳跃式取样法放置0.1 m2调查框,取样5次。采集调查框内所有新梢,统计茶蚜为害和未为害的新梢数量,计算茶蚜危害率;使用毛笔收集新梢上茶蚜并称重,估算茶蚜数量。对于茶蚜数量估算,采用随机抽样的方法获得茶蚜百头重,取3次平均值作为基准茶蚜重量。茶蚜危害率和茶蚜数量依据下列公式计算。
茶蚜危害率(%)=茶蚜为害新梢/所有新梢×100% 茶蚜数量(头)/m2=0.1m2茶蚜重量/基准茶蚜重量(g)×100×10 1.2.2 苯丙氨酸解氨酶、多酚氧化酶酶活和脯氨酸含量的测定
以茶蚜未为害组EN和茶蚜为害组EA为材料,使用苯丙氨酸解氨酶(PAL)检测试剂盒测定PAL活性,使用多酚氧化酶(PPO)活性检测试剂盒测定PPO活性,使用脯氨酸(Pro)含量检测试剂盒测定Pro含量,操作方法均参照试剂盒说明书,试剂盒购于北京盒子生工科技有限公司。
1.2.3 主要化学物质含量测定
以EN和EA为材料,采用蒽酮-硫酸比色法测定总水溶性碳水化合物的含量,采用三氯化铝比色法测定黄酮类化合物总量[18]。同时,参照国家标准GB/T8313-2018《茶叶中茶多酚和儿茶素类含量的检测方法》测定茶多酚含量。
1.2.4 广泛靶向代谢物组学分析
(1)样品提取。EN和EA样品在冻干机真空冷冻干燥后研磨成粉末,精确称取0.1 g粉末,加入1 mL 70 %甲醇涡旋30 s,间隔30 min涡旋一次,重复6次后于4 ℃过夜。提取液12 000 r/min离心10 min,上清用0.22 μm微孔滤膜过滤后保存于进样瓶,用于超高效液相色谱偶联串联质谱分析(Ultra-performance liquid chromatography-tandem mass spectrometry,UPLC-MS/MS)。
(2)UPLC-MS/MS分析。UPLC和MS/MS分析分别使用Shim-pack UFLC SHIMADZU CBM30A(日本岛津)和AB SCIEX QTRAP® 4500 + (美国AB SCIEX)。代谢物使用UPLC分级,色谱柱为Waters ACQUITY UPLC HSS T3 C18柱(1.8 µm粒径,2.1 mm内径,100 mm长),流动相A相为含0.1%甲酸的超纯水,B相为含0.1%甲酸的乙腈。洗脱梯度设置为A∶B(95∶5)0 min,A∶B (5∶95)10.0 min,A∶B(5∶95)11.0 min,A∶B(95∶5)11.1 min,A∶B(95∶5)15.0 min,流速、柱温和进样量分别维持在0.4 mL/min、40 ℃和2 μL。
代谢物经由UPLC分离后被注入电喷雾离子源,电离后进入QTRAP® 4500 + 质谱仪分析。电喷雾电离温度550 ℃,使用三重四极杆(Qtrap)对代谢物母离子及其二级碎片进行检测和分析,相关参数设置如下:质谱正电压和负电压为5500 V和−4500 V、离子源气体Ⅰ和气体Ⅱ为55 psi和60 psi、气帘气25 psi、碰撞诱导电离为高。代谢物定量利用Qtrap的多反应监测模式,具体过程为:Qtrap筛选出目标物质母离子,母离子经碰撞池断裂成碎片离子,碎片离子再进入Qtrap进行二级质谱分析并筛选出特征碎片离子。
(3)代谢物定性和定量分析。利用软件Analyst 1.6.3处理质谱数据。基于苏州帕诺米克生物医药科技有限公司自建数据库(Biodeep database),据二级质谱对代谢物进行定性分析。使用MultiaQuant软件对所有物质质谱峰进行峰面积积分,并对同一代谢物在不同样本中的质谱出峰进行积分校正,每个色谱峰的峰面积代表对应物质的相对含量。
1.3 数据分析
采用SIMCA-P 14.1软件进行主成分分析(Principal component analysis,PCA)和正交偏最小二乘法判别分析(Orthogonal partial least squares-discriminant analysis,OPLS-DA)。采用SPSS 19.0软件进行单因素方差分析(ANOVA),P < 0.05(*) 为显著差异,P < 0.01 (**)为极显著差异,P < 0.001(***)表示差异极显著,ns为差异不显著。使用 GraphPad Prism 5 软件制作柱状图。
2. 结果与分析
2.1 茶蚜对‘鄂茶一号’危害情况分析
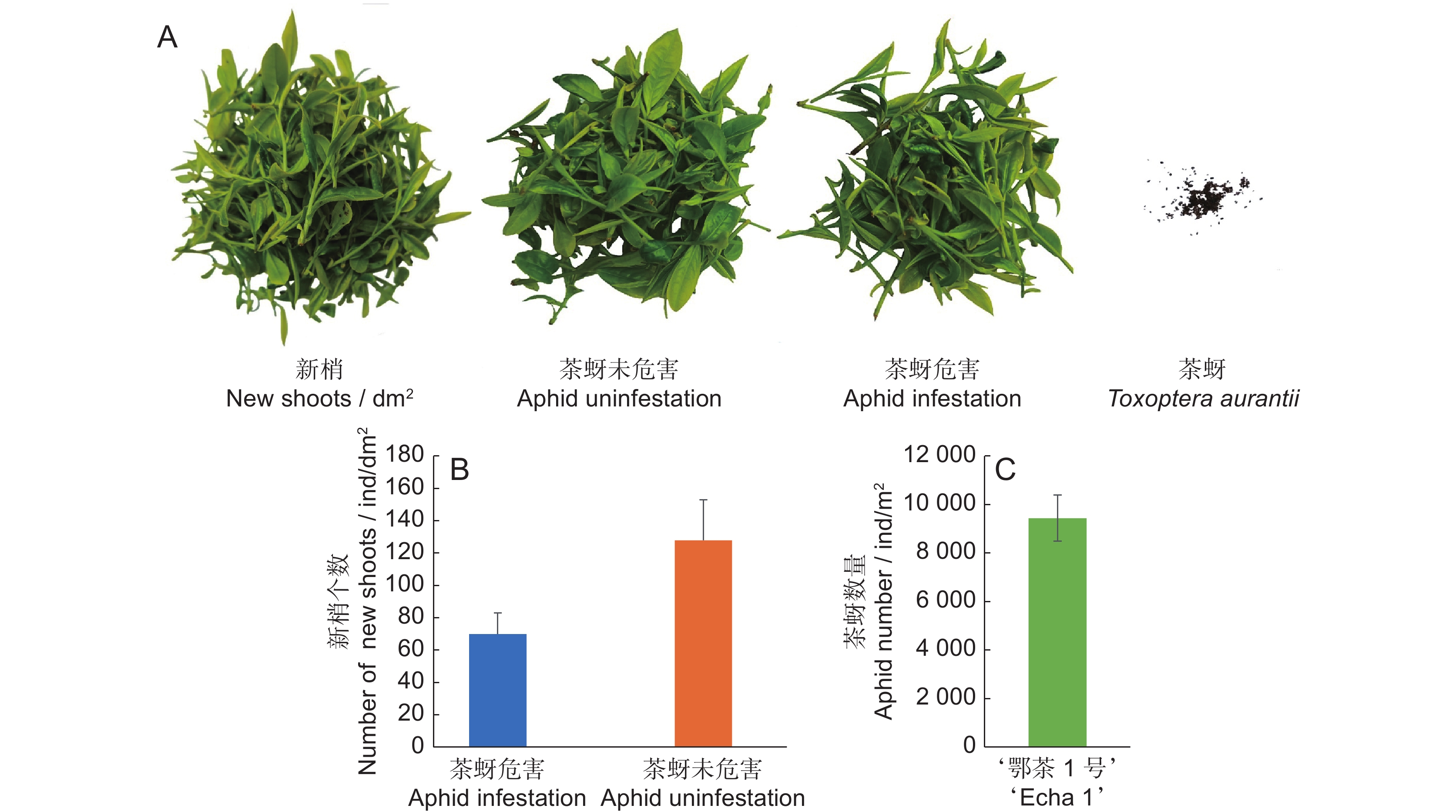
采取0.1 m2 ‘鄂茶一号’采摘面内当年生全部新梢,分析茶蚜危害情况(图1:A)。结果发现,茶蚜新梢危害率高达35.4%(图1:A、B),1 m2采摘面上约有9 500头茶蚜(图1:C)。据棉花蚜害的5级分级标准(GB/T 22101.2-2009),认定‘鄂茶一号’受害程度为2级,即有蚜虫、受害最严重叶片皱缩不展,表明‘鄂茶一号’对茶蚜中等抗性。
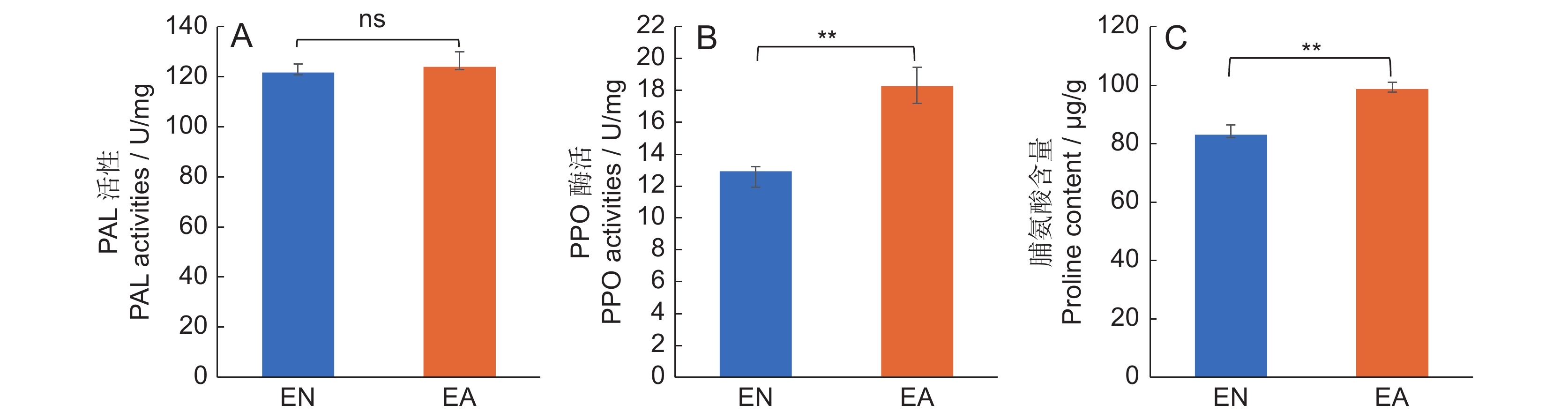
2.2 茶蚜危害对PAL、PPO活力及Pro含量的影响
PAL和PPO是植物防御虫害的两种主要酶类[19]。本实验中,茶蚜危害后PAL活性仅极轻微上升(图2:A),而 PPO活性显著上升(图2:B),表明茶蚜危害诱导了PAL和PPO 活性上调。
Pro参与植物防御各种生物和非生物胁迫[20]。为了探讨Pro在茶树防御茶蚜中的作用,测定了EN和EA中Pro的含量。结果发现,EA中Pro含量极显著高于EN(图2:C),表明茶蚜为害诱导了茶树新梢中Pro增加,Pro参与茶树防御茶蚜危害。
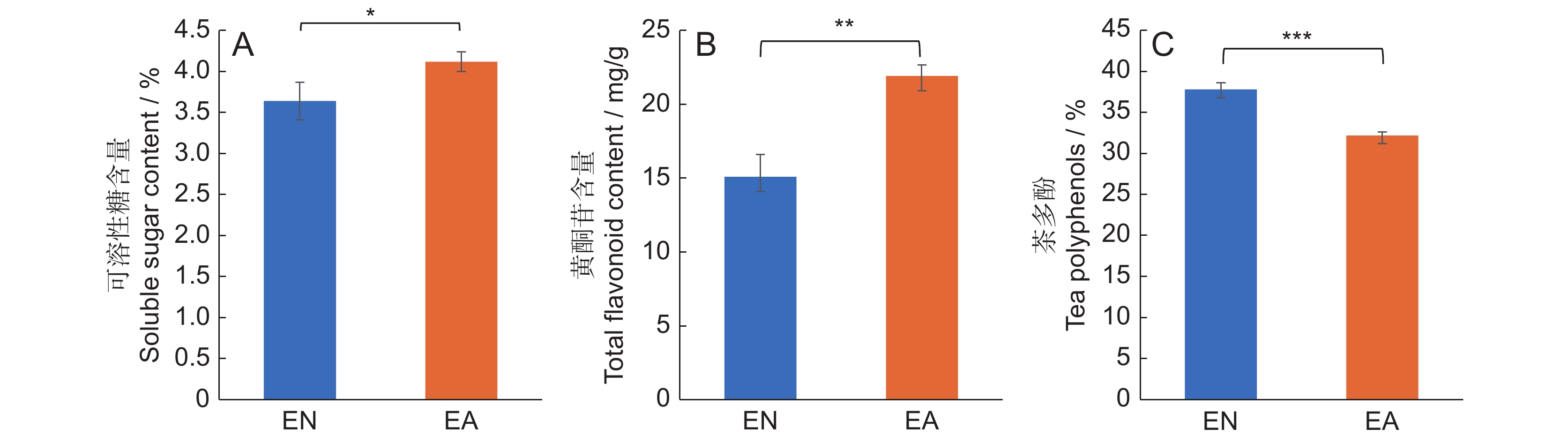
2.3 茶蚜危害对主要代谢物含量的影响
茶多酚和糖类是茶树叶片中的主要化学成分,黄酮是茶多酚的一种组分。为了了解茶蚜取食对茶树新梢中主要代谢物的影响,本研究测定了可溶性糖、茶多酚和总黄酮的含量。茶叶中黄酮类物质大部分以黄酮苷形式存在,因此以黄酮苷含量表示黄酮类总量。研究结果显示,与EN相比,在茶蚜取食的EA中可溶性糖和总黄酮含量显著上升(图3:A、B),而茶多酚含量却极显著下降(图3:C)。
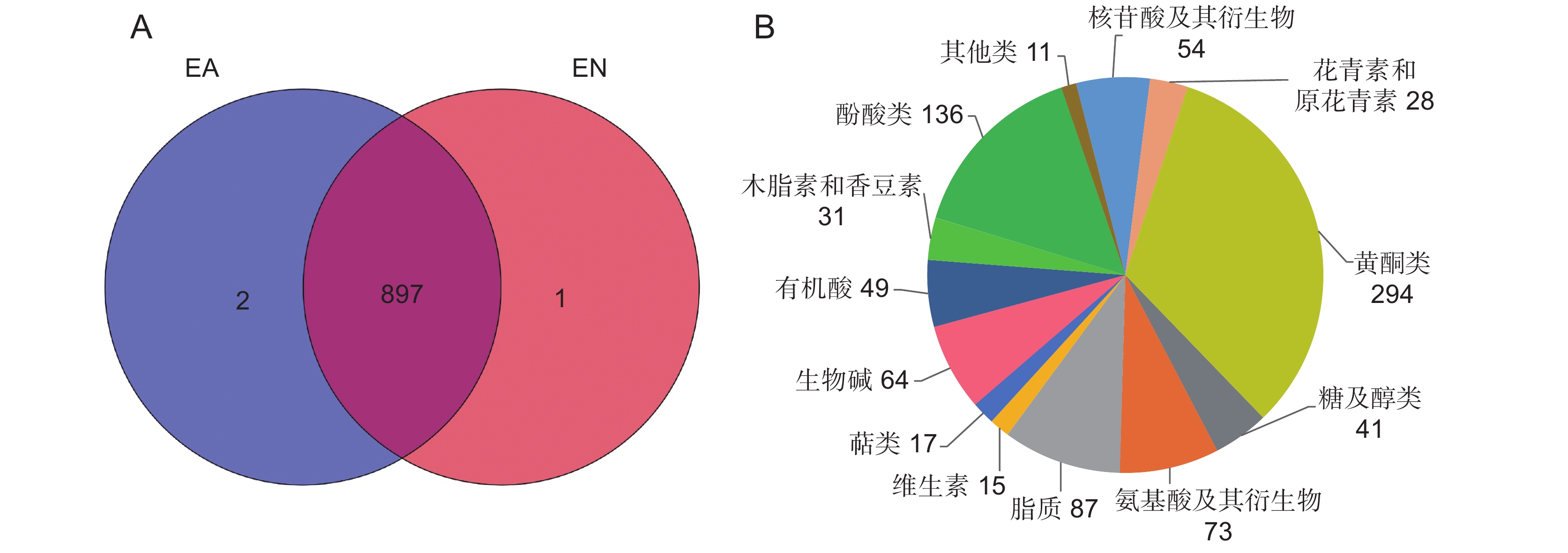
2.4 茶蚜为害下茶树新梢代谢组分析
经过广泛靶向代谢组分析,在EN和EA中共鉴定出900种代谢物。其中,在EN中鉴定到898 种,在EA中鉴定到 899 种,二者共有897 种(图4:A)。鉴定的代谢物中有初级代谢产物270个,包括41个糖及醇类物质、54个核苷酸及其衍生物、73个氨基酸及其衍生物、87个脂质类物质和15个维生素;次级代谢产物630个,包括294个黄酮类化合物、136个酚酸类化合物、64个生物碱、49个有机酸、31个木脂素和香豆素、28个花青素和原花青素、17个萜类物质和11个其他类物质(图4:B)。
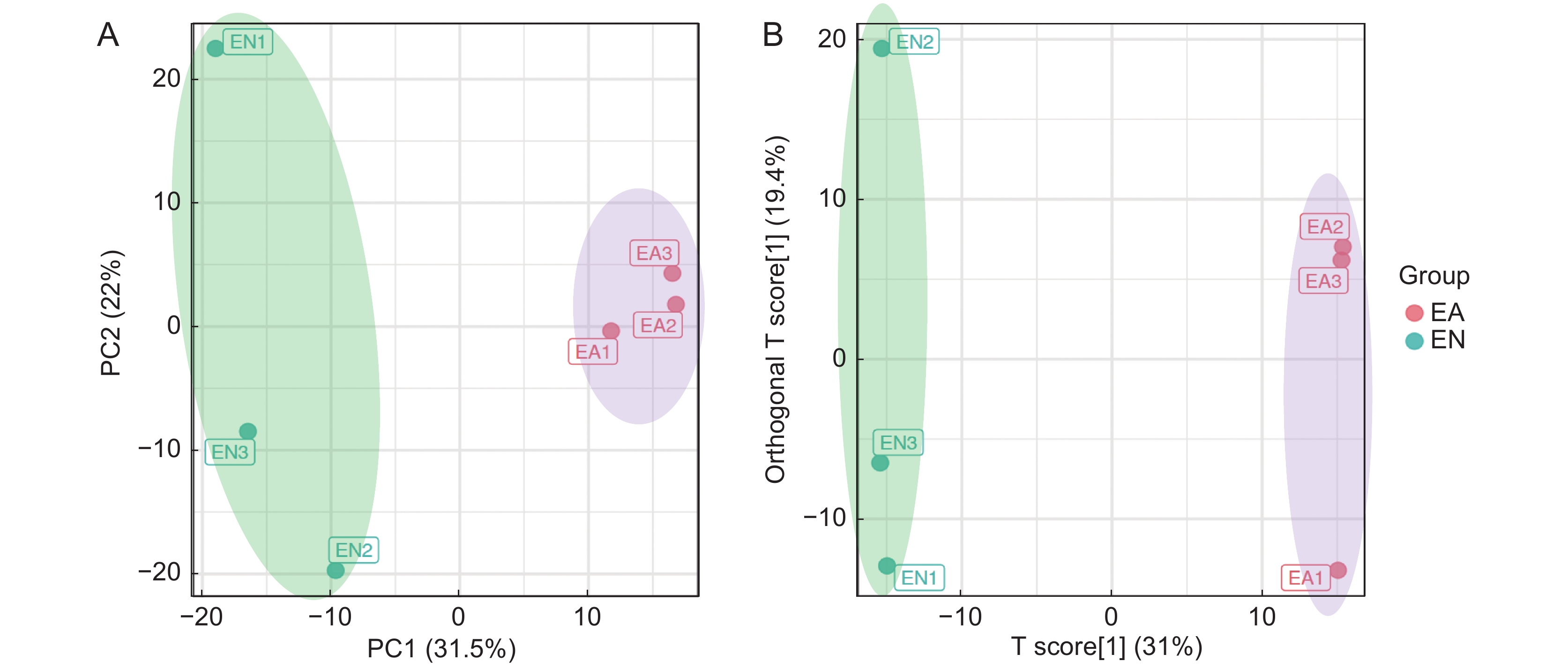
2.5 代谢物PCA 和OPLS-DA分析
为了评估EN和EA间代谢物差异和组内样品的变异度,对样品进行PCA分析(图5:A)。其中,第1主成分(PC1)贡献率为 31.5%,第2主成分(PC2)贡献率为 22.0%,两种主成分贡献率之和为 53.5%,表明两个主成分基本能够反映茶树新梢样品的主要特征信息。EA和EN在PC1上分离较远,表明茶蚜为害导致‘鄂茶一号’新梢代谢物发生了显著变化。EA组3次重复聚集较近,表明组内3个样本重复性好;EN组3次重复聚集相对较远,样品重复性一般,这可能与随机取样位置有关。
为了进一步挖掘EN和EA间代谢物差异,对样品进行了OPLS-DA模型分析。建立的OPLS-DA模型参数Q2=0.751,说明此模型是有效模型,可以预测和解释茶蚜为害和未为害的新梢代谢物差异。OPLS-DA模型得分结果与PCA基本一致(图5:B),即EA和EN分离较好,再次表明茶蚜为害导致‘鄂茶一号’茶树新梢代谢物发生了显著变化。
2.6 茶蚜为害下茶树新梢差异代谢物分析
为了精确地筛选出差异代谢物质,本研究采用差异倍数(Fold change,FC)和 OPLS-DA的变量重要性投影(Variable importance in projection, VIP)2个指标筛选差异代谢物质,选定FC ≥ 2或 ≤ 0.5和VIP ≥ 1的代谢物为显著差异代谢物(Significantly differentially accumulated metabolites,DAM)。经过筛选,在EN和EA中共鉴定到8个DAM,包括 N-乙酰-β-D-甘露糖胺、L-鸟氨酸、3-羟基硬脂酸、HHDP-glucose isomer、川陈皮素、桔皮素、槲皮素-3-O-(2''-O-没食子酰)-β-D-葡萄糖苷和茉莉酸-异亮氨酸(表1)。
表 1 茶蚜为害下茶树新梢显著差异代谢物质Table 1. Significantly differentially accumulated metabolites identified from EN and EA编号
Index物质
Compound分类
ClassVIP EA/EN 倍数
EA/EN fold-change初级代谢物 kz001031 N-乙酰-β-D-甘露糖胺 多糖衍生物 1.80 150.67 kz000007 L-鸟氨酸 氨基酸 1.77 2.09 kz005414 3-羟基硬脂酸 游离脂肪酸 1.77 3.65 次级代谢物 kz002532 HHDP-glucose isomer 原花青素 1.79 0.021 kz005216 川陈皮素 黄酮 1.77 0.49 kz005232 桔皮素Tangeretin 黄酮醇 1.30 0.17 kz001739 槲皮素-3-O-(2''-O-没食子酰)-β-D-葡萄糖苷 黄酮醇 1.79 124.30 kz000308 茉莉酸-异亮氨酸 有机酸 1.74 2.84 根据功能不同,8个DAM可分为初级代谢物(3个)和次生代谢物(5个)。初级代谢物可进一步分为多糖衍生物(1个)、氨基酸(1个)和游离脂肪酸(1个);次生代谢物也可进一步分为类黄酮(4个)和有机酸(1个)。在茶蚜为害的EA中, 3个初级代谢物全部上调表达,5个次生代谢物中2个显著上调表达,3个显著下调表达。
3. 讨论
3.1 PAL和PPO在茶树防御茶蚜中的作用
PAL和PPO是植物次生代谢途径上的两个关键酶。其中,PAL是苯丙烷类代谢途径的关键酶和限速酶,调控类黄酮、植保素、木质素等次生代谢产物的合成。PPO是一类广泛存在的含铜金属酶,催化酚类物质氧化成醌类物质。研究发现,PAL和PPO 活性与植物抗蚜能力呈高度正相关,且活性受蚜虫取食的诱导[14-17]。芦屹等[14]报道,棉花(Gossypium herbaceum L.)PAL和PPO 活性受棉蚜取食诱导,且两种酶在抗蚜品种中的活性显著高于感蚜品种。马荣金等[15]发现,高抗蚜黄瓜(Cucumis sativus L.)PAL和PPO 活性均显著高于其他品种,而在抗蚜黄瓜中PPO 和PAL活性并未共同作用,多数品种PPO 活性高于感蚜品种,少数品种PAL活性高于感蚜品种。本研究中,茶蚜为害的EA中PAL活性小幅上升,PPO活性显著上升,表明PPO在‘鄂茶一号’防御茶蚜过程中起重要作用。
3.2 类黄酮化合物参与茶树防御茶蚜
本研究在EN和EA中共鉴定到8个DAM,其中4个DAM包括HHDP-glucose isomer、槲皮素-3-O-(2''-O-没食子酰)-β-D-葡萄糖苷、川陈皮素和桔皮素属于黄酮类化合物(类黄酮),占比50%,表明类黄酮化合物在‘鄂茶一号’抵御茶蚜危害中具有重要作用。类黄酮化合物是茶树体内的一类次生代谢物,根据C环修饰不同,可分为黄酮、黄酮醇、黄烷酮、异黄酮、黄烷醇和花青素6大类。本研究中鉴定的槲皮素-3-O-(2''-O-没食子酰)-β-D-葡萄糖苷和桔皮素属于黄酮醇,川陈皮素属于黄酮,而HHDP-glucose isomer属于原花青素。
研究表明,类黄酮化合物中黄酮、黄酮醇、原花青素和花青素作为抗氧化剂具有减少或清除活性氧的作用,参与植物响应多种非生物胁迫,如盐[21, 22]、干旱和氧化胁迫[23],黄酮、黄酮醇和花青素还参与植物抵御生物胁迫如病菌侵染[24]、食草动物侵扰[25],及蚜虫取食[1, 7, 15]。在本研究鉴定的4个类黄酮化合物中,槲皮素-3-O-(2''-O-没食子酰)-β-D-葡萄糖苷在茶蚜危害后的EA中显著上调表达,其他3个显著下调表达。值得提及的是,槲皮素-3-O-(2''-O-没食子酰)-β-D-葡萄糖苷仅在EA中检出,而HHDP-glucose isomer仅在EN中检出,表明此2种物质是茶蚜为害的响应物质,在‘鄂茶一号’响应茶蚜为害过程中发挥关键作用,但是它们的具体功能尚有待进一步研究。至于槲皮素-3-O-(2''-O-没食子酰)-β-D-葡萄糖苷是茶蚜为害时新梢新合成还是从其他部位运输过来还有待进一步验证。
此外,总黄酮含量测定结果表明茶蚜诱导了‘鄂茶一号’新梢中黄酮苷含量显著增加,这可能与槲皮素-3-O-(2''-O-没食子酰)-β-D-葡萄糖苷产生有关。类似的,Golawska等[26, 27]也报道蚜虫取食诱导了黄酮苷物质的合成,且黄酮苷含量与蚜虫生长呈负相关。由此可见,类黄酮是一种蚜虫防御物质,类黄酮含量增加也是茶树防御茶蚜的一种响应。至于4种类黄酮化合物的差异表达,推测它们的功能在于维持‘鄂茶一号’体内总黄酮含量处于一种稳定的平衡状态,既能使茶蚜获取营养,又防御茶蚜大量繁殖。
另外,研究也发现茶蚜为害的EA中茶多酚含量极显著下降,这应该与PAL和PPO活性变化密切相关。茶蚜为害后,PAL和PPO活性变化导致EA中催化合成的酚类物质增幅不大,而氧化生成的醌类物质却显著增多,致使茶多酚含量极显著下降。醌类物质的增加,降低了茶蚜对植物营养的利用,延缓或阻碍茶蚜的生长发育和繁殖,也是茶树应对茶蚜的一种抵御策略。
3.3 激素信号激活茶树防御茶蚜系统
JA-Ile是一种茉莉酸类植物生长调节物质,其作为最主要的活性JA与其共受体结合启动JA核心信号途径[28]。JA信号通路主要调控植物对生物和非生物胁迫的防御反应,尤其作为环境信号分子介导植物防御外力损伤和病原体感染[29]。现已证实,JA也是植物防御蚜虫最重要的激素信号分子,一般情况下,JA正向调控植物对蚜虫的防御[30, 31]。JA促进植物防御蚜虫已在拟南芥(Arabidopsis thaliana (L.) Heynh.)[32, 33]、蒺藜苜蓿(Medicago truncatula Gaertn.)[34]、豌豆(Pisum sativum L.)[11]、大豆(Glycine max (L.) Merr.)[29]、土豆(Solanum tuberosum L.)[35]和小麦(Triticum aestivum L.)[4]等植物中报道。
本研究中,JA-Ile在茶蚜为害的‘鄂茶一号’新梢中显著上调表达,表明JA介导的信号防御途径被激活,这有助于茶树重新调动下游防御系统和抵御茶蚜危害。Yates-Stewart等[36]的研究发现,JA-Ile在无毒蚜虫为害的抗性大豆中显著富集,且外源应用减少了有毒蚜虫在抗性大豆上的群体数量,证实JA-Ile参与植物防御蚜虫。与之不同,Grover等[37]在探讨蚜虫为害下不同高梁(Sorghum bicolor (L.) Moench)品系的激素响应时发现,与未接种蚜虫相比,蚜虫接种7 d时不同品系中JA-Ile含量无显著差异,抗性品系中JA含量显著增加,敏感性品系中JA前体物质(12-氧-植物二烯酸)含量显著减少,而SA含量显著增加,表明JA和SA分别在抗性品系和敏感性品系响应蚜虫为害中发挥作用。综上,在植物受到蚜虫攻击时,JA或者SA防御信号途径的激活取决于不同植物甚至是同种植物不同品系,JA信号途径也可由不同的JA类物质激活。本研究中,‘鄂茶一号’对茶蚜的防御由JA-Ile介导的JA信号途径激活,但在其他茶树品种中是否发挥作用有待开展进一步研究。
3.4 脯氨酸参与茶树防御茶蚜
L-鸟氨酸是植物体内Pro和多胺合成的前体物质[38],Pro和多胺是已知的参与植物防御多种非生物和生物胁迫的化学物质[39]。本研究中,L-鸟氨酸、 Pro和2种多胺(精胺和腐胺)在EN中组成性表达,在茶蚜为害的EA中L-鸟氨酸显著上调表达(2.09倍),Pro上调了1.46倍,而精胺和腐胺仅呈现了极轻微的表达差异,分别是1.02倍和0.99倍。此结果表明L-鸟氨酸和Pro在EA中协同上调表达,茶蚜为害下茶树新梢中L-鸟氨酸倾向于合成Pro。同样,冉伟[5]在探讨茶蚜对‘龙井43’叶片危害时发现,Pro在茶蚜为害2 d时显著上调表达(1.45倍)。综上,茶蚜取食诱导茶树中Pro表达量上调,表明Pro可能是茶树防御茶蚜的重要化学物质。
为了进一步探讨Pro在茶树防御茶蚜中的作用,我们测定了Pro的含量。结果发现,在茶蚜为害的‘鄂茶一号’新梢中,Pro含量也显著增加,再次表明Pro是茶蚜为害下茶树的响应物质。研究表明,Pro在植物应对蚜虫刺吸胁迫中具重要作用,且Pro含量与植物的抗蚜性呈正相关[14, 40-43]。吴梅梅等[40]研究发现,4种西瓜(Citrullus lanatus (Thunb.) Matsum. & Nakai)幼苗叶片的Pro含量在蚜虫取食后均显著提高,且抗蚜材料Pro含量显著高于感蚜材料。Xu等[43]在探讨蚜虫胁迫下6种小麦的生化响应时发现,蚜虫取食后小麦Pro含量显著增加,且抗蚜小麦Pro含量明显高于感蚜小麦。同样,芦屹等[14]在研究棉花对棉蚜危害响应时也发现,Pro含量在抗蚜棉花中较高且在棉蚜为害时被显著诱导。由此可见,Pro是植物防御蚜虫危害的重要物质,Pro含量可作为一个检测植物防御蚜虫能力强弱的指标。
3.5 初生代谢物质为茶蚜生存提供营养
糖类、氨基酸和游离脂肪酸是茶树体内主要的营养物质,能为茶蚜的生存和繁殖提供能量。然而,研究发现植物中组成性的高糖含量不利于蚜虫生长[44]。由此可见,植物体内可溶性糖对蚜虫具有双重作用,即为蚜虫提供营养,又因高浓度高渗透具抑制作用。本研究中,茶蚜为害后,EA中可溶性总糖含量显著提升。与我们的结果不同,Xu等[43]研究发现感蚜小麦在蚜虫为害后可溶性糖含量显著下降,抗蚜小麦也轻微下调。吴梅梅等[40]也报道,抗蚜西瓜幼苗可溶性总糖含量显著低于感蚜材料,且在蚜虫取食后显著下降。综上,在不同植物响应蚜虫取食时,可溶性糖的变化因植物品种而异。
此外,代谢组分析结果显示,N-乙酰-β-D-甘露糖胺(糖类衍生物)、3-羟基硬脂酸(游离脂肪酸)和L-鸟氨酸(氨基酸)在茶蚜为害的EA中均显著上调表达,可能改善了茶蚜食物的营养品质,利于或妨碍茶蚜存活,也为‘鄂茶一号’对茶蚜中等抗性提供了解释。
4. 结论
茶蚜是春季茶树新梢的主要害虫之一,研究茶蚜为害下茶树新梢代谢物的变化有利于筛选和培育抗蚜茶树品种。本研究以茶蚜为害和未为害的‘鄂茶一号’茶树新梢为材料,开展了广泛的靶向代谢组学研究和主要代谢物定量分析。代谢组学研究共鉴定到8个DAM,3个参与初生代谢的DAM分别是多糖衍生物、氨基酸和游离脂肪酸,它们的上调表达可能为茶树防御化合物提供合成前体,也可能改变了茶蚜生存所需的营养物质和能量;5个参与次生代谢的DAM是防御信号物质和类黄酮物质,信号物质上调激活茶树防御途径,促使下游代谢物变化,而类黄酮作为防御物质直接参与防御茶蚜危害。代谢物定量分析发现,茶蚜为害下 ‘鄂茶一号’新梢中可溶性糖、黄酮和Pro含量上升,而茶多酚含量下降,进一步证实了茶树诱导防御物质合成来抑制茶蚜严重危害。同时,研究发现茶蚜为害诱导了PAL和PPO酶活上调,参与黄酮和茶多酚含量变化的调控。综上,我们认为JA-Ile、类黄酮和Pro是‘鄂茶一号’防御茶蚜危害的主要物质。
-
表 1 茶蚜为害下茶树新梢显著差异代谢物质
Table 1 Significantly differentially accumulated metabolites identified from EN and EA
编号
Index物质
Compound分类
ClassVIP EA/EN 倍数
EA/EN fold-change初级代谢物 kz001031 N-乙酰-β-D-甘露糖胺 多糖衍生物 1.80 150.67 kz000007 L-鸟氨酸 氨基酸 1.77 2.09 kz005414 3-羟基硬脂酸 游离脂肪酸 1.77 3.65 次级代谢物 kz002532 HHDP-glucose isomer 原花青素 1.79 0.021 kz005216 川陈皮素 黄酮 1.77 0.49 kz005232 桔皮素Tangeretin 黄酮醇 1.30 0.17 kz001739 槲皮素-3-O-(2''-O-没食子酰)-β-D-葡萄糖苷 黄酮醇 1.79 124.30 kz000308 茉莉酸-异亮氨酸 有机酸 1.74 2.84 -
[1] Jakobs R,Schweiger R,Müller C. Aphid infestation leads to plant part-specific changes in phloem sap chemistry,which may indicate niche construction[J]. New Phytol,2019,221 (1):503−514. doi: 10.1111/nph.15335
[2] Lan H,Zhang ZF,Wu J,Cao HH,Liu TX. Performance and transcriptomic response of the English grain aphid,Sitobion avenae,feeding on resistant and susceptible wheat cultivars[J]. J Integr Agric,2021,20 (1):178−190. doi: 10.1016/S2095-3119(20)63349-4
[3] Züst T,Agrawal AA. Mechanisms and evolution of plant resistance to aphids[J]. Nat Plants,2016,2 (1):15206. doi: 10.1038/nplants.2015.206
[4] Leybourne DJ,Valentine TA,Robertson JAH,Pérez-Fernández E,Main AM,et al. Defence gene expression and phloem quality contribute to mesophyll and phloem resistance to aphids in wild barley[J]. J Exp Bot,2019,70 (15):4011−4026. doi: 10.1093/jxb/erz163
[5] 冉伟. 基于代谢组学的蚜虫为害降低茶树对茶尺蠖的抗性机制研究[D]. 北京: 中国农业科学院, 2018: 13-17. [6] 范元兰. 长尖叶蔷薇响应蔷薇长管蚜胁迫的转录组与代谢组分析[D]. 昆明: 云南大学, 2021: 55-56. [7] 闫乐乐,卜璐璐,牛良,曾文芳,鲁振华,等. 广泛靶向代谢组学解析桃蚜危害对桃树次生代谢产物的影响[J]. 中国农业科学,2022,55(6):1149−1158. Yan LL,Bu LL,Niu L,Zeng WF,Lu ZH,et al. Widely targeted metabolomics analysis of the effects of Myzus persicae feeding on Prunus persica secondary metabolites[J]. Scientia Agricultura Sinica,2022,55 (6):1149−1158.
[8] Stolpe C,Giehren F,Krӓmer U,Müller C. Both heavy metal-amendment of soil and aphid-infestation increase Cd and Zn concentrations in phloem exudates of a metal-hyperaccumulating plant[J]. Phytochemistry,2017,139:109−117. doi: 10.1016/j.phytochem.2017.04.010
[9] Morkunas I,Mai VC,Gabryś B. Phytohormonal signaling in plant responses to aphid feeding[J]. Acta Physiol Plant,2011,33 (6):2057−2073. doi: 10.1007/s11738-011-0751-7
[10] Mai VC,Bednarski W,Borowiak-Sobkowiak B,Wilkaniec B,Samardakiewicz S,Morkunas I. Oxidative stress in pea seedling leaves in response to Acyrthosiphon pisum infestation[J]. Phytochemistry,2013,93:49−62. doi: 10.1016/j.phytochem.2013.02.011
[11] Mai VC,Drzewiecka K,Jeleń H,Narożna D,Rucińska-Sobkowiak R,et al. Differential induction of Pisum sativum defense signaling molecules in response to pea aphid infestation[J]. Plant Sci,2014,221-222:1−12. doi: 10.1016/j.plantsci.2014.01.011
[12] Liang DN,Liu M,Hu QJ,He M,Qi XH,et al. Identification of differentially expressed genes related to aphid resistance in cucumber (Cucumis sativus L.)[J]. Sci Rep,2015,5 (1):9645. doi: 10.1038/srep09645
[13] Luo J,Wei K,Wang SH,Zhao WY,Ma CR,et al. COI1-regulated hydroxylation of Jasmonoyl-L-isoleucine impairs Nicotiana attenuata’s resistance to the generalist herbivore Spodoptera litura[J]. J Agric Food Chem,2016,64 (14):2822−2831. doi: 10.1021/acs.jafc.5b06056
[14] 芦屹,王惠卿,陈刘生,王佩玲,李晶. 新疆棉花品种次生代谢酶活性与诱导抗蚜性的关系[J]. 植物保护,2017,43(4):51−55. doi: 10.3969/j.issn.0529-1542.2017.04.009 Lu Y,Wang HQ,Chen LS,Wang PL,Li J. Correlation between induced resistance to aphids and secondary metabolism enzyme activities of cotton varieties in Xinjiang[J]. Plant Protection,2017,43 (4):51−55. doi: 10.3969/j.issn.0529-1542.2017.04.009
[15] 马荣金,李田田,刘桂军,曹辰兴. 不同黄瓜材料抗蚜性与部分次生代谢物及其相关酶活力的关系[J]. 中国农学通报,2015,31(19):80−86. doi: 10.11924/j.issn.1000-6850.casb15010197 Ma RJ,Li TT,Liu GJ,Cao CX. The relationship between aphid-resistance of different cucumber materials and part of secondary metabolites and their related enzyme activities[J]. Chinese Agricultural Science Bulletin,2015,31 (19):80−86. doi: 10.11924/j.issn.1000-6850.casb15010197
[16] 王蔓. 苹果黄蚜取食和水杨酸处理诱导的苹果苗对山楂叶螨和苹果全爪螨的影响[D]. 泰安: 山东农业大学, 2020: 5-7. [17] Kaur R,Gupta AK,Taggar GK. Induced resistance by oxidative shifts in pigeonpea (Cajanus cajan L. ) following Helicoverpa armigera (Hübner) herbivory[J]. Pest Manag Sci,2015,71 (5):770−782. doi: 10.1002/ps.3851
[18] 商业部茶叶畜产局商业部杭州茶叶加工研究所. 茶叶品质理化分析[M]. 上海: 上海科学技术出版社, 1989: 340-350. [19] 郭祖国,王梦馨,崔林,韩宝瑜. 6种防御酶调控植物体应答虫害胁迫机制的研究进展[J]. 应用生态学报,2018,29(12):4248−4258. Guo ZG,Wang MX,Cui L,Han BY. Research progress on the underlying mechanisms of plant defense enzymes in response to pest stress[J]. Chinese Journal of Applied Ecology,2018,29 (12):4248−4258.
[20] Trovato M, Forlani G, Signorelli S, Funck D. Proline metabolism and its functions in development and stress tolerance[M]//Hossain MA, Kumar V, Burritt DJ, Fujita M, Mäkelä PSA, eds. Osmoprotectant-Mediated Abiotic Stress Tolerance in Plants. Cham: Springer, 2019: 41-72.
[21] Bian XH,Li W,Niu CF,Wei W,Hu Y,et al. A class B heat shock factor selected for during soybean domestication contributes to salt tolerance by promoting flavonoid biosynthesis[J]. New Phytol,2020,225 (1):268−283. doi: 10.1111/nph.16104
[22] Song ZH,Yang Q,Dong BY,Li N,Wang MY,et al. Melatonin enhances stress tolerance in pigeon pea by promoting flavonoid enrichment,particularly luteolin in response to salt stress[J]. J Exp Bot,2022,73 (17):5992−6008. doi: 10.1093/jxb/erac276
[23] Nakabayashi R,Yonekura-Sakakibara K,Urano K,Suzuki M,Yamada Y,et al. Enhancement of oxidative and drought tolerance in Arabidopsis by overaccumulation of antioxidant flavonoids[J]. Plant J,2014,77 (3):367−379. doi: 10.1111/tpj.12388
[24] Margaria P,Ferrandino A,Caciagli P,Kedrina O,Schubert A,et al. Metabolic and transcript analysis of the flavonoid pathway in diseased and recovered Nebbiolo and Barbera grapevines (Vitis vinifera L. ) following infection by Flavescence dorée phytoplasma[J]. Plant Cell Environ,2014,37 (9):2183−2200. doi: 10.1111/pce.12332
[25] Dong NQ,Lin HX. Contribution of phenylpropanoid metabolism to plant development and plant-environment interactions[J]. J Integr Plant Biol,2021,63 (1):180−209. doi: 10.1111/jipb.13054
[26] Goławska S,Łukasik I,Goławskir A,Kapusta I,Janda B. Alfalfa (Medicugo sutiva L. ) apigenin glycosides and their effect on the pea aphid (Acyrthosiphon pisum)[J]. Polish J Environ Stud,2010,19 (5):913−919.
[27] Goławska S,Łukasik I. Antifeedant activity of luteolin and genistein against the pea aphid,Acyrthosiphon pisum[J]. J Pest Sci,2012,85 (4):443−450. doi: 10.1007/s10340-012-0452-z
[28] Li MY,Yu GH,Cao CL,Liu P. Metabolism,signaling,and transport of jasmonates[J]. Plant Commun,2021,2 (5):100231. doi: 10.1016/j.xplc.2021.100231
[29] Wang FF,Yu GH,Liu P. Transporter-mediated subcellular distribution in the metabolism and signaling of jasmonates[J]. Front Plant Sci,2019,10:390. doi: 10.3389/fpls.2019.00390
[30] Zhuang HF,Li J,Song J,Hettenhausen C,Schuman MC,et al. Aphid (Myzus persicae) feeding on the parasitic plant dodder (Cuscuta australis) activates defense responses in both the parasite and soybean host[J]. New Phytol,2018,218 (4):1586−1596. doi: 10.1111/nph.15083
[31] Chapman KM,Marchi-Werle L,Hunt TE,Heng-Moss TM,Louis J. Abscisic and jasmonic acids contribute to soybean tolerance to the soybean aphid (Aphis glycines Matsumura)[J]. Sci Rep,2018,8 (1):15148. doi: 10.1038/s41598-018-33477-w
[32] Ellis C,Karafyllidis L,Turner JG. Constitutive activation of jasmonate signaling in an Arabidopsis mutant correlates with enhanced resistance to Erysiphe cichoracearum,Pseudomonas syringae,and Myzus persicae[J]. Mol Plant Microbe Interact,2002,15 (10):1025−1030. doi: 10.1094/MPMI.2002.15.10.1025
[33] De Vos M,Kim JH,Jander G. Biochemistry and molecular biology of Arabidopsis-aphid interactions[J]. BioEssays,2007,29 (9):871−883. doi: 10.1002/bies.20624
[34] Gao LL,Anderson JP,Klingler JP,Nair RM,Edwards OR,Singh KB. Involvement of the octadecanoid pathway in bluegreen aphid resistance in Medicago truncatula[J]. Mol Plant Microbe Interact,2007,20 (1):82−93. doi: 10.1094/MPMI-20-0082
[35] Kerchev PI,Fenton B,Foyer CH,Hancock RD. Infestation of potato (Solanum tuberosum L.) by the peach-potato aphid (Myzus persicae Sulzer) alters cellular redox status and is influenced by ascorbate[J]. Plant Cell Environ,2012,35 (2):430−440. doi: 10.1111/j.1365-3040.2011.02395.x
[36] Yates-Stewart AD,Pekarcik A,Michel A,Blakeslee JJ. Jasmonic acid-isoleucine (JA-Ile) is involved in the host-plant resistance mechanism against the soybean aphid (Hemiptera:Aphididae)[J]. J Econ Entomol,2020,113 (6):2972−2978. doi: 10.1093/jee/toaa221
[37] Grover S,Agpawa E,Sarath G,Sattler SE,Louis J. Interplay of phytohormones facilitate sorghum tolerance to aphids[J]. Plant Mol Biol,2022,109 (4-5):639−650. doi: 10.1007/s11103-020-01083-y
[38] 赵福庚,孙诚,刘友良,章文华. 盐胁迫下大麦幼苗多胺与脯氨酸合成竞争前体L-Arg[J]. 作物学报,2001,27(5):622−626. Zhao FG,Sun C,Liu YL,Zhang WH. The biosyntheses of polyamines and proline competed for precursor L-Arginine in barley seedlings under salt stress[J]. Acta Agronomica Sinica,2001,27 (5):622−626.
[39] Zarattini M,Forlani G. Toward unveiling the mechanisms for transcriptional regulation of proline biosynthesis in the plant cell response to biotic and abiotic stress conditions[J]. Front Plant Sci,2017,8:927. doi: 10.3389/fpls.2017.00927
[40] 吴梅梅,杨丽荣,杨小振,张显,马建祥,等. 蚜虫侵染对西瓜幼苗生理生化指标的影响[J]. 果树学报,2015,32(5):943−949. Wu MM,Yang LR,Yang XZ,Zhang X,Ma JX,et al. Effect of aphid invasion on physiological and biochemical indexes in watermelon seedling stage[J]. Journal of Fruit Science,2015,32 (5):943−949.
[41] 邓小霞,江海澜,彭俊,何泽敏,马天文,王俊刚. 花铃期棉花对棉蚜刺吸胁迫的生理响应[J]. 应用昆虫学报,2013,50(1):161−166. Deng XX,Jiang HL,Peng J,He ZM,Ma TW,Wang JG. Physiological responses of cotton to feeding by Aphis gossypii during the flower-bolling stage[J]. Chinese Journal of Applied Entomology,2013,50 (1):161−166.
[42] Kumar A,Yadav S,Ahlawat N,Yadav J. Biochemical basis of resistance to mustard aphid Lipaphis erysimi (Kaltenbach)[J]. Indian J Entomol,2020,82 (4):875−879. doi: 10.5958/0974-8172.2021.00027.4
[43] Xu LJ,Hou QL,Zhao YJ,Ni ZF,Liang HZ,Liang RQ. Biochemical responses of resistant and susceptible wheat cultivars to English grain aphid (Sitobio avenae F. ) at grain-filling stage[J]. Acad J Biotechnol,2016,4 (7):276−284.
[44] Douglas AE. The nutritional physiology of aphids[J]. Adv Insect Physiol,2003,31:73−140.
-
期刊类型引用(2)
1. 蔡晓明,边磊,罗宗秀,李兆群,修春丽,付楠霞,陈宗懋. 2023年茶树病虫害防控研究进展. 中国茶叶. 2024(10): 1-7 .  百度学术
百度学术
2. 李东洋,马驰宇,陈瑶. 除虫菊素Ⅰ和Ⅱ在茶叶上的残留动态. 农技服务. 2024(10): 53-58 .  百度学术
百度学术
其他类型引用(0)



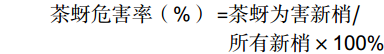
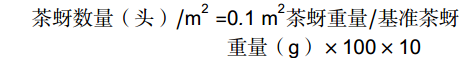
 下载:
下载: