Effect of ascorbic acid oxidation inhibition on growth of Oryza sativa L. seedlings under abscisic acid (ABA) treatment
-
摘要:
抗坏血酸(AsA)氧化是调节抗坏血酸稳态的重要生物学过程,但该过程的生物学效应及其是否受脱落酸(ABA)调节尚不清楚。本研究以水稻(Oryza sativa L.)抗坏血酸氧化基因OsAAO4为对象,分析其对ABA的响应特性,及其敲除系在ABA处理下的表型与生理特性。结果显示,OsAAO4具有丰富的ABA响应元件,ABA处理9 h后,其在根和幼叶中的表达量达到峰值。未经ABA处理时,OsAAO4敲除系KO-1、KO-2的株高、存活率与野生型(‘中花11’)均无显著差异;在ABA处理下,两个敲除系的株高分别比野生型降低38.34%和25.72%,存活率下降21.91%和5.48%,幼苗抗坏血酸氧化酶(AAO)活性下降35.31%和31.81%,脱氢抗坏血酸(DHA)含量下降29.72%和26.95%,而AsA含量则分别提高27.17%和16.37%。转录组学分析发现,在ABA处理下,KO-1和野生型的差异表达基因显著富集于氧化还原和氧化应激途径。研究结果表明OsAAO4介导的抗坏血酸氧化是维持逆境胁迫下AsA氧化还原稳态并确保幼苗正常生长的重要生理机制。
Abstract:Ascorbic acid (AsA) oxidation is a critical biological process involved in maintaining ascorbic acid homeostasis. However, its regulation by abscisic acid (ABA) and associated biological effects remain unknown. This study selected OsAAO4, an ascorbate oxidase gene in rice (Oryza sativa L.), to analyze its response to ABA and the phenotypic and physiological effects of its knockout under ABA treatment. Results showed that OsAAO4 contained abundant ABA response elements and reached peak expression levels in roots and young leaves after 9 h of ABA treatment, increasing 13.8-fold and 7.4-fold, respectively. Under normal conditions without ABA treatment, there were no significant differences in plant height and survival rate between the wild-type (‘Zhonghua 11’) and OsAAO4 knockout lines (KO-1 and KO-2). However, exposure to 10 μmol/L ABA resulted in significant reductions in plant height (38.34% in KO-1 and 25.72% in KO-2) and survival rate (21.91% in KO-1 and 5.48% in KO-2) compared to wild-type rice. Additionally, in young leaves, the knockout lines exhibited decreased ascorbic acid oxidase (AAO) activity (35.31% in KO-1 and 31.81% in KO-2) and dehydroascorbic acid (DHA) content (29.72% in KO-1 and 26.95% in KO-2), while AsA content increased (27.17% in KO-1 and 16.37% in KO-2). Transcriptomic analysis revealed that differentially expressed genes (DEGs) between KO-1 and wild-type rice under ABA treatment were significantly enriched in pathways involved in redox homeostasis and oxidative stress. These findings suggest that ascorbic acid oxidation mediated by OsAAO4 plays an important role in maintaining AsA homeostasis and ensuring the normal growth of rice seedlings under ABA treatment.
-
Keywords:
- Oryza sativa /
- Ascorbic acid /
- Ascorbic acid oxidase /
- OsAAO4 /
- Abscisic acid
-
抗坏血酸(Ascorbic acid,AsA),又称维生素C,为多羟基小分子化合物,能直接清除自由基或通过酶促反应来清除活性氧(Reactive oxygen species,ROS),是氧化还原系统的重要组分[1]。研究表明,提高总抗坏血酸含量可以增强植物耐逆性[2]。抗坏血酸稳态受抗坏血酸氧化酶(Ascorbic acid oxidase,AAO)的调节。AAO属于多铜氧化酶类,负责将还原型抗坏血酸转化为氧化态脱氢抗坏血酸(Dehydroascorbic acid,DHA),从而维持细胞内AsA还原态和氧化态间的平衡[3]。AsA在线粒体中合成,约10%的AsA借助转运体输出到质外体[4]。质外体是感受并传导环境变化信号的重要部位,当AAO活性升高时,抗坏血酸库的氧化还原比升高,导致质膜两侧的氧化还原梯度发生改变[5]。在拟南芥(Arabidopsis thaliana (L.) Heynh)中,这种变化能调节气孔开闭、胁迫响应和基因表达,进而影响生长发育[6, 7]。
据预测,水稻(Oryza sativa L.)AAO基因家族含有OsAAO1~OsAAO5 5个成员[8]。研究表明,OsAAO1~OsAAO4的基因产物定位在质外体中[9]。过表达OsAAO2可促进抗坏血酸氧化,导致还原型AsA减少,ROS积累增加,使水稻对盐敏感[7]。突变OsAAO4(OsORAP1)降低了水稻体内超氧阴离子的含量,提高了水稻耐臭氧的能力[10],说明抑制质外体抗坏血酸氧化有助于缓解胁迫。此外,也有研究指出AAO在抵御生物或非生物逆境中具有积极作用,如OsAAO3和OsAAO4通过结合MoAo1抑制稻瘟病菌侵染[11];体外喷施抗坏血酸氧化酶和DHA增强了对根结线虫的抵抗能力[12],为认识质外体抗坏血酸氧化的生物学功能提供了新视角。
脱落酸(ABA)响应型基因的表达调控是介导植物非生物胁迫反应的重要机制[13]。研究发现,在干旱、高温、盐等诱导基因的启动子区域中存在ABA反应元件(Abscisic acid-responsive element,ABRE),且ABRE位点与ABA诱导的某些转录因子活性呈正相关[14]。目前,尽管已报道水稻AAO的表达受干旱、高温等的诱导[15],但是不同家族成员对胁迫条件下植物生长发育的作用尚缺乏深入研究。为此,本文以OsAAO4为研究对象,分析了敲除OsAAO4的水稻表型与生理特性,研究结果旨在揭示抗坏血酸氧化过程在响应胁迫及维持生长发育中的作用。
1. 材料与方法
1.1 水稻AAO家族基因启动子的顺式作用元件分析
使用PlantCARE(http://bioinformatics.psb.uegnt.be/webtools/plantcare/html/)在线工具,预测AAO家族基因5个成员启动子区域(起始密码子上游2 kb)中的顺式作用元件类型和数量,分析其ABA响应元件,这些基因分别为:OsAAO1(LOC_Os06g37080)、OsAAO2(LOC_Os06g37150)、OsAAO3(LOC_Os07g02810)、OsAAO4(LOC_Os09g20090)和OsAAO5(LOC_Os09g32952)。
1.2 OsAAO4基因对ABA的响应分析
将粳稻(Oryza sativa subsp. japonica Kato.)‘中花11’(ZH11)发芽种子置于木村B营养液中培养至一叶一心期,光照强度为594 µmol·m−2·s−1,光照12 h,温度28 ℃;黑暗12 h,温度26 ℃,相对湿度80%。然后,将幼苗转入含10 μmol/L ABA的木村B营养液中进行处理。采用Trizol法,提取处理0、1、3、6、9、12和24 h后根与幼叶的总RNA。利用HiScript®Ⅲ ALL-in-one RT SuperMix Perfect for qPCR试剂盒(南京诺唯赞)将RNA反转录成cDNA,使用SYBR Green Ⅰ嵌合荧光法(南京诺唯赞)进行实时荧光定量反应。表达检测引物为OsAAO4-F:5′-GGGACATCAGCTACCAGTTC-3′,OsAAO4-R:5′-GCTCGTTGTAGAAGGTGT-3′。以OsActin为内参基因(OsActin-F:5′-CGGTGTCATGGTCGGAAT-3′,OsActin-R:5′-GCTCGTTGTAGAAGGTGT-3′),ABA处理0 h为对照,按照2−ΔΔCT法分析基因的相对表达量。
1.3 OsAAO4敲除系构建及纯系筛选
OsAAO4基因包含2个外显子和1个内含子,CDS全长2 112 bp,编码577个氨基酸。利用CRISPR direct(http://crispr.dbcls.jp/)在线工具,在OsAAO4的第1外显子495~517 bp处设计靶点,序列为5′-ACACCGTGCTGCTCAACGACTGG-3′。将以CRISPR -Cas9为骨架的敲除载体Cas9-OsAAO4转入‘中花11’中,利用特异性引物KO-OsAAO4 F/R(5′-ATCGTCGTCAACGTCAAGAACTC-3′,5′-TGCCCCTCGATCTCGAAGTTGA-3′)对转化单株进行扩增与测序,鉴定靶位点发生杂合或纯合突变的单株,经加代获得纯系。
1.4 OsAAO4敲除系的株高与存活率分析
将‘中花11’和敲除纯系KO-1、KO-2在木村B营养液中培养至一叶一心期后,进行ABA处理。将不同体积的母液加入4 L营养液中,配制含0、10、20和30 μmol/L ABA的水培液;每个处理组72棵苗,每组3次重复,培养条件同前。处理14 d(每隔5 d更换一次营养液)后观察幼苗生长情况,采用SPSS 26.0软件进行单因素方差分析和显著性检验(P<0.05),分析敲除系和野生型的株高与存活率差异。
1.5 OsAAO4敲除系抗坏血酸途径的生理指标
10 μmol/L ABA处理‘中花11’和敲除系幼苗3 d,取根和叶片样品各0.1 g,测定AAO酶活性(上海茁彩生物试剂盒)、还原型抗坏血酸AsA含量(苏州科铭生物试剂盒)以及脱氢抗坏血酸DHA含量(优选生物试剂盒)。每个处理3次生物学重复,采用SPSS 26.0软件进行单因素方差分析和显著性检验(P<0.05),比较OsAAO4敲除系和野生型之间的差异。
1.6 OsAAO4敲除系和野生型差异表达基因分析
以对照‘中花11’和OsAAO4敲除系KO-1的一叶一心期幼苗为实验材料, 10 μmol/L ABA处理0和9 h后,各取0.1 g叶片,提取总RNA,利用Illumina HiSeq高通量测序技术进行转录组测序。以|log2(FoldChange)|>1,P-adj<0.05为差异表达基因标准,利用GO(Gene Ontology,http://www.geneontology.org/)和KEGG(Kyoto Encyclopedia of Genes and Genomes, http://www.kegg.jp)在线软件,分析正常情况和ABA处理下KO-1与对照组差异表达基因的富集特点。
2. 结果与分析
2.1 AAO家族启动子元件分析
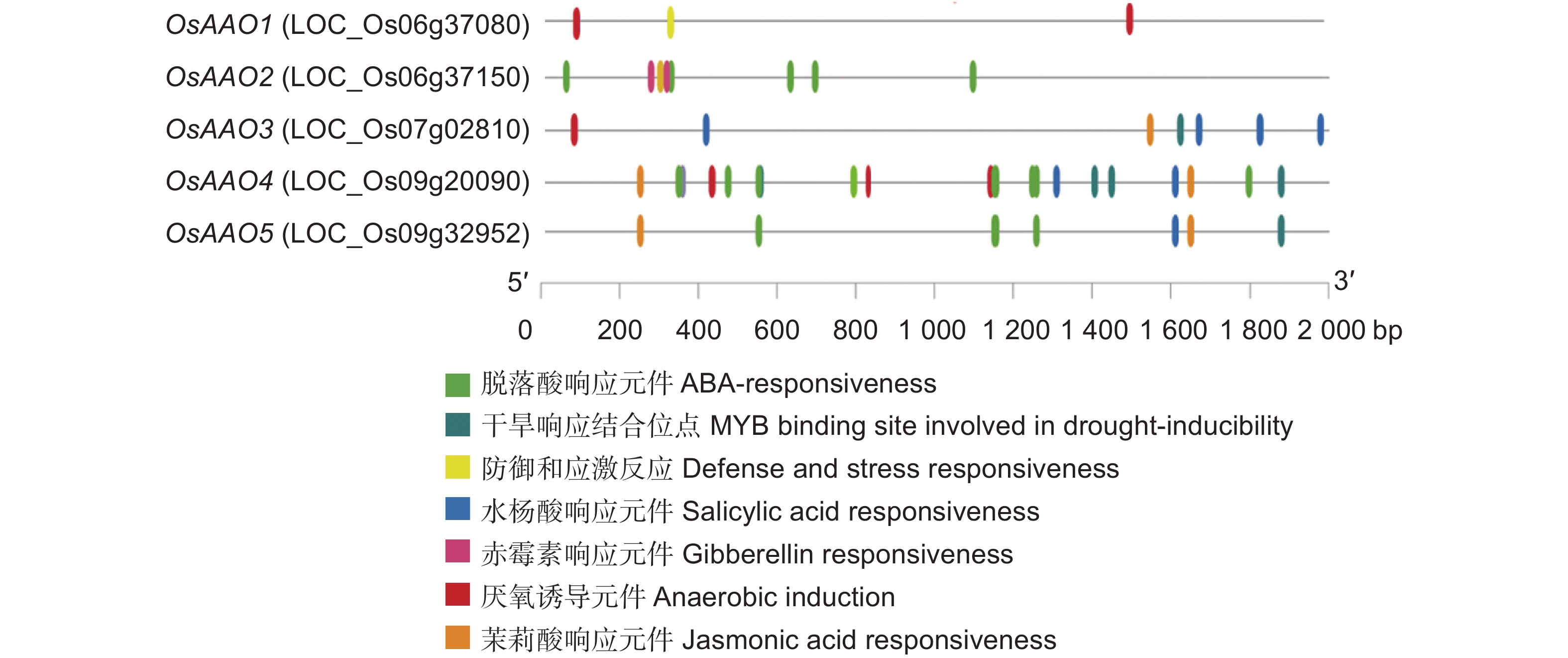
Plant CARE分析发现,AAO家族的5个成员启动子上均含有多个与逆境和激素响应相关的顺式作用元件,包括脱落酸响应元件(ABA-responsiveness,ABRE)、防御和应激反应(Defense and stress responsiveness)、赤霉素响应元件(Gibberellin-responsiveness)、干旱响应结合位点(MYB binding site involved in drought-inducibility)、厌氧诱导元件(Anaerobic induction)以及茉莉酸响应元件(Salicylic acid responsiveness)和水杨酸响应元件(MeJA-responsiveness)(图1),表明AAO基因可能具有非生物逆境调节功能。相比而言,OsAAO4启动子上的ABRE较丰富,共有9个,在各区段都有分布,以1 200~1 251 bp区段居多,推测该基因的表达受脱落酸诱导。
2.2 OsAAO4基因表达量分析
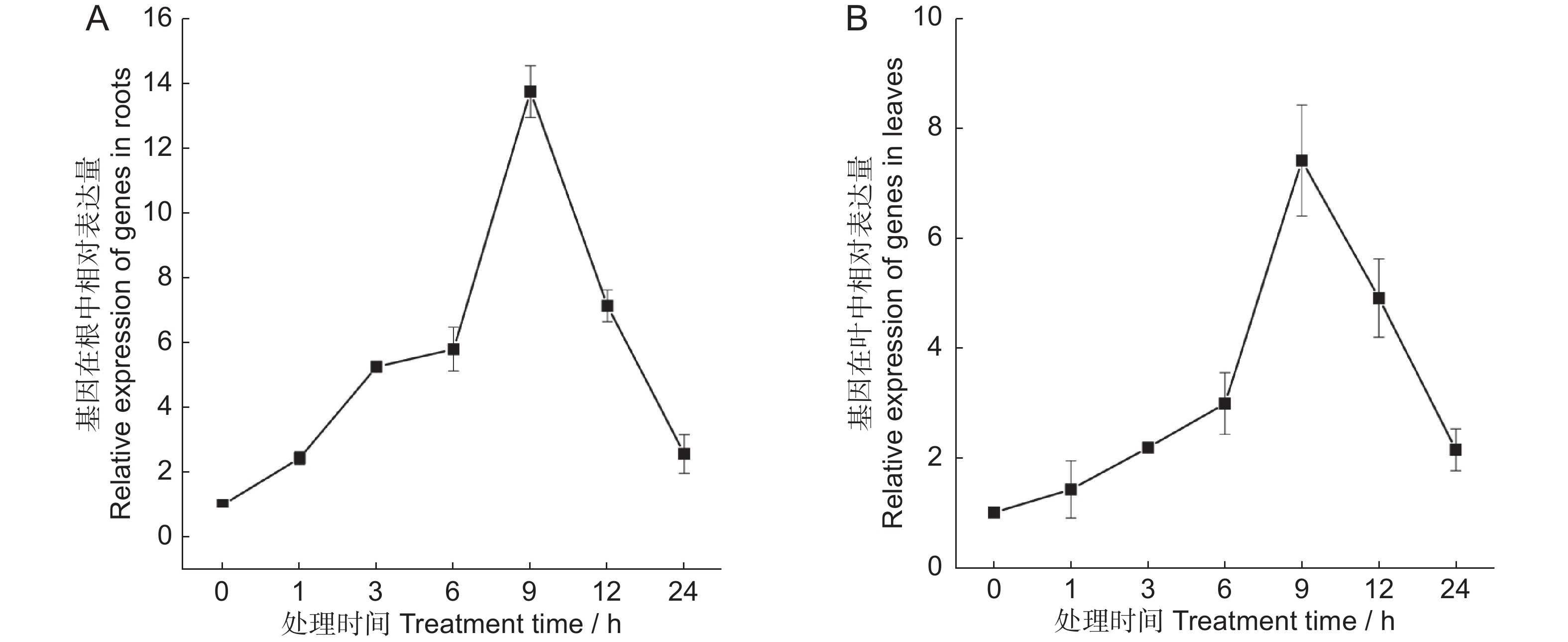
利用RT-qPCR分析水稻OsAAO4对ABA的响应特点,结果显示,ABA处理24 h内,根和幼叶中OsAAO4的表达量均呈先升后降趋势,在处理9 h后达到峰值,分别为0 h的13.8倍和7.4倍,表明OsAAO4的表达受ABA诱导(图2)。
2.3 OsAAO4敲除系的获得及纯系鉴定
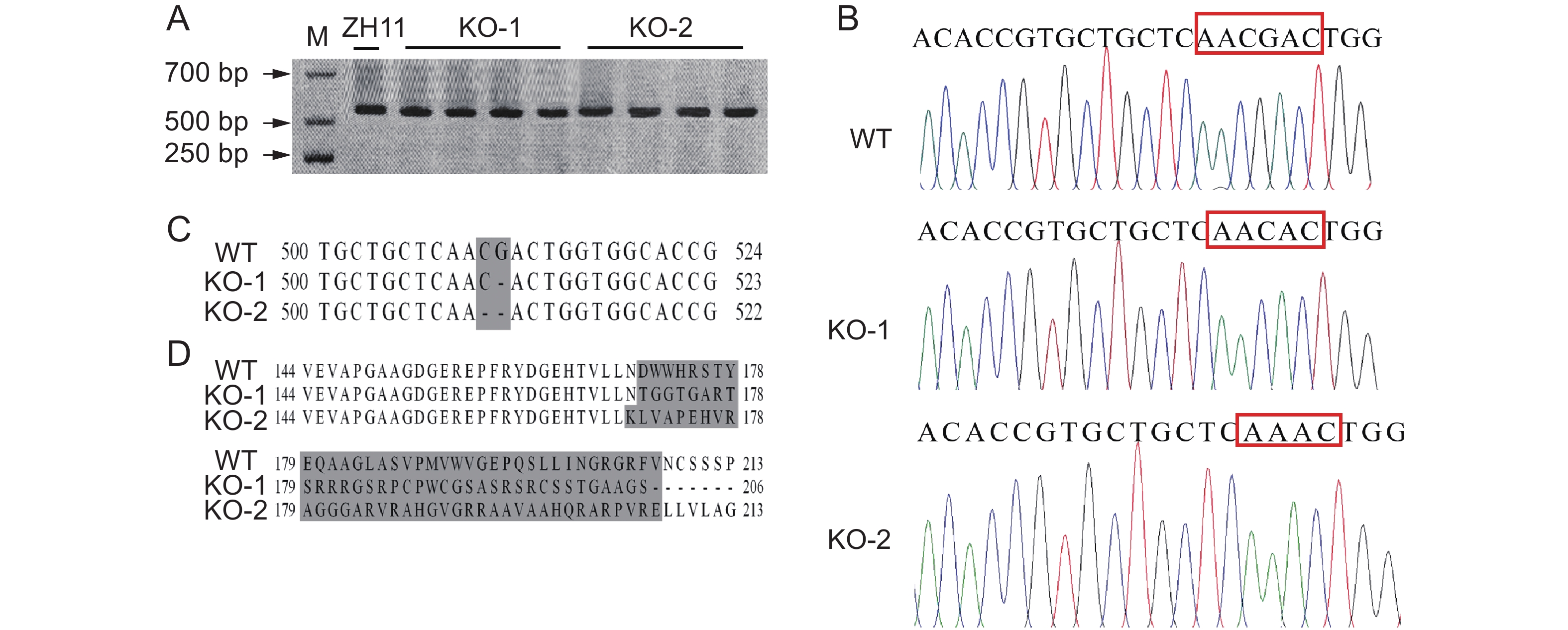
利用农杆菌介导法将OsAAO4敲除载体Cas9-OsAAO4转化至‘中花11’中,获得了11个再生植株;特异性引物扩增及测序分析表明,获得了靶位点突变单株。通过加代繁殖,获得了T3代纯系KO-1和KO-2。与野生型相比,KO-1和KO-2分别缺失了1个碱基G和两个碱基CG(图3:A、B)。碱基缺失将导致KO-1和KO-2的OsAAO4基因发生移码突变,产生没有功能的蛋白产物(图3:C、D)。
2.4 OsAAO4敲除系的株高与存活率分析
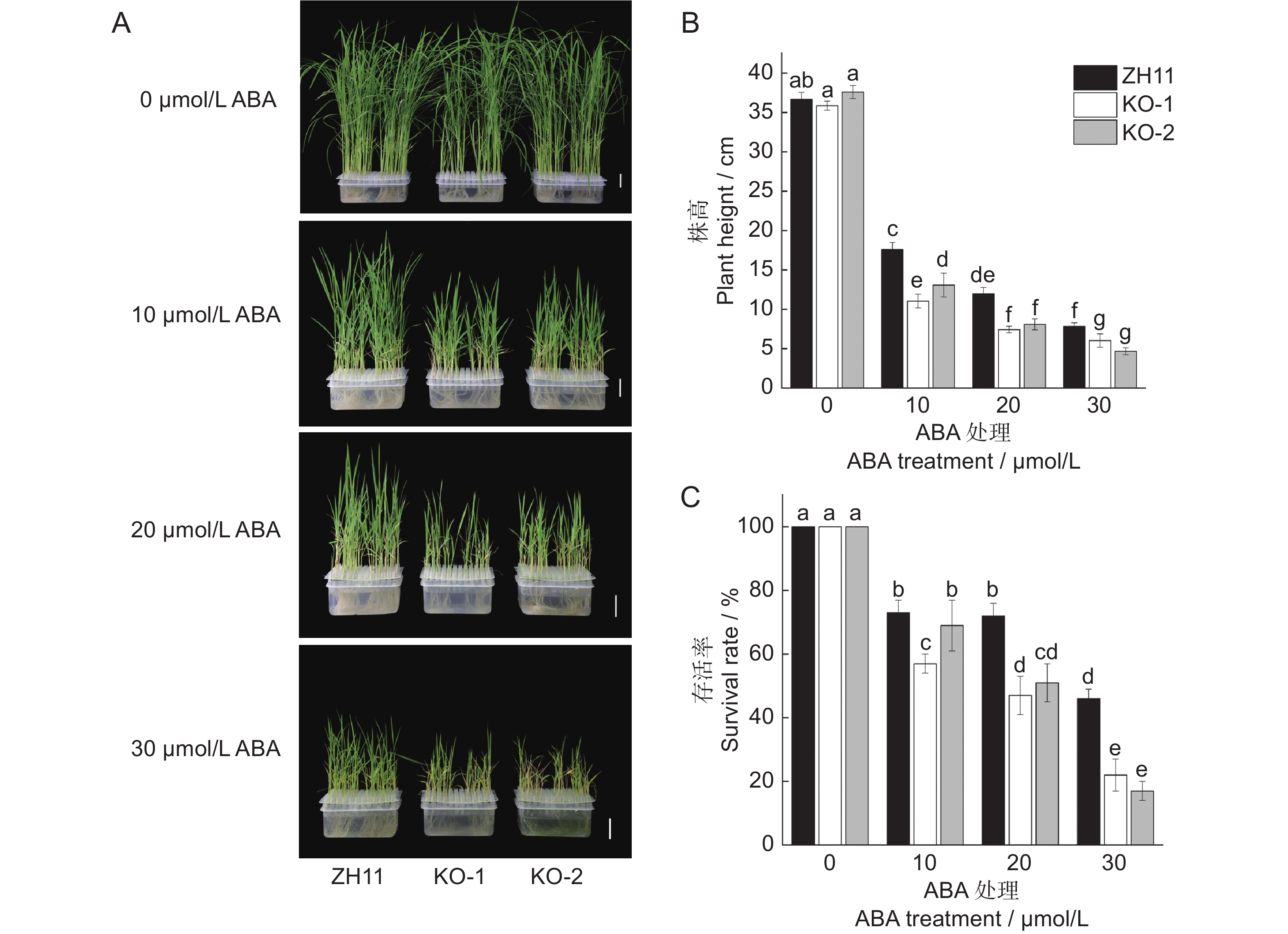
当ABA为0 μmol/L时,OsAAO4敲除系和野生型的生长势一致。施用10、20或30 μmol/L的ABA处理14 d后,敲除系的生长势明显低于野生型(图4:A)。ABA浓度为10 μmol/L时, KO-1、KO-2的株高分别比野生型下降38.34%和25.72%,存活率分别下降21.91%和5.48%。ABA浓度为20 μmol/L时,KO-1和KO-2的部分叶片枯黄,株高较野生型分别下降38.11%和32.53%,存活率降低了34.74%和29.16%。当ABA浓度升为30 μmol/L时,KO-1和KO-2植株的大部分叶片枯死,株高分别降低22.80%和40.33%,存活率分别降低52.17%和63.04%。这些现象表明敲除OsAAO4增强了水稻对ABA的敏感性(图4:B、C)。
![]() 图 4 OsAAO4敲除系与野生型(ZH11)幼苗长势(A)、株高(B)与存活率(C)的比较不同小写字母表示OsAAO4敲除系与野生型间差异显著(P<0.05)。下同。Figure 4. Growth (A), plant height (B), and survival rate (C) of OsAAO4 knockout and wild-type lines under ABA treatmentDifferent lowercase letters indicate significant differences between OsAAO4 knockout lines and wild-type at 0.05 level. Same below.
图 4 OsAAO4敲除系与野生型(ZH11)幼苗长势(A)、株高(B)与存活率(C)的比较不同小写字母表示OsAAO4敲除系与野生型间差异显著(P<0.05)。下同。Figure 4. Growth (A), plant height (B), and survival rate (C) of OsAAO4 knockout and wild-type lines under ABA treatmentDifferent lowercase letters indicate significant differences between OsAAO4 knockout lines and wild-type at 0.05 level. Same below.2.5 AAO酶活、AsA与DHA的含量及其比值分析
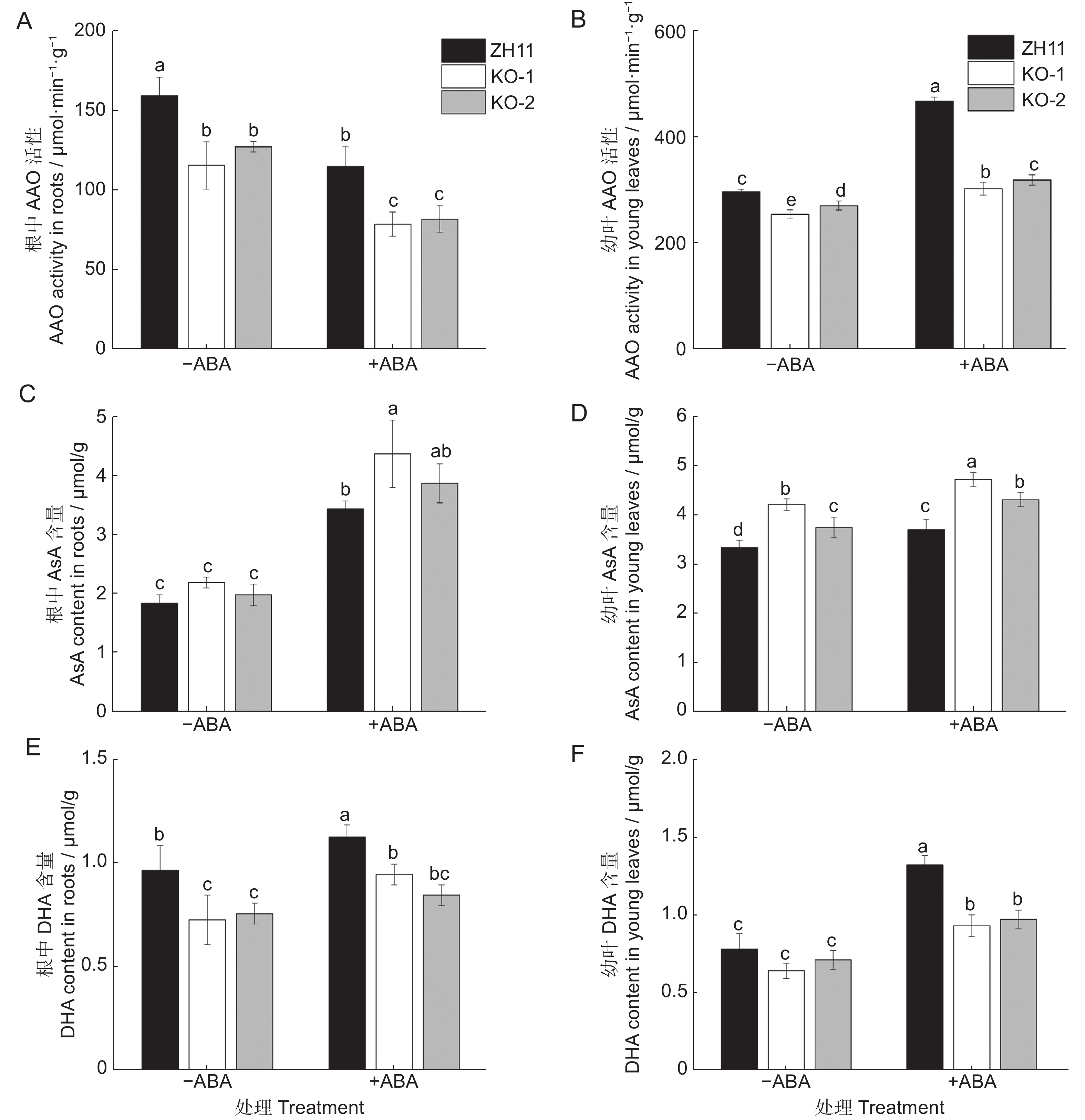
在野生型水稻中,ABA处理后,根和幼叶中的AAO酶活分别呈现降低和增强的趋势。和野生型相比,敲除系的AAO活性显著下降;未经ABA处理时,KO-1和KO-2根的AAO活性分别比野生型低27.41%和20.07%,幼叶的AAO活性分别低14.31%和8.66%。10 μmol/L ABA处理3 d后,KO-1和KO-2植株根的AAO活性分别下降了31.43%和28.60%,幼叶中的活性则分别降低了35.31%和31.81%(图5:A、B)。
受AAO活性下降的影响,敲除系KO-1和KO-2植株中AsA的含量上升,DHA的含量下降,AsA/DHA值升高。未经ABA处理时,KO-1和KO-2根中的AsA含量分别比野生型高19.18%和7.71%,在幼叶中分别高26.06%和11.94%(图5:C、D),根中的DHA含量分别比野生型低24.14%和21.38%,在幼叶中低14.31%和8.66%(图5:E、F)。ABA处理3 d后,KO-1和KO-2根中的AsA含量分别升高了26.94%和12.53%,幼叶中分别升高了27.17%和16.37%(图5:C、D),而DHA含量在根中分别下降了16.47%和25%,在幼叶中分别下降了29.72%和26.95%(图5:E、F)。
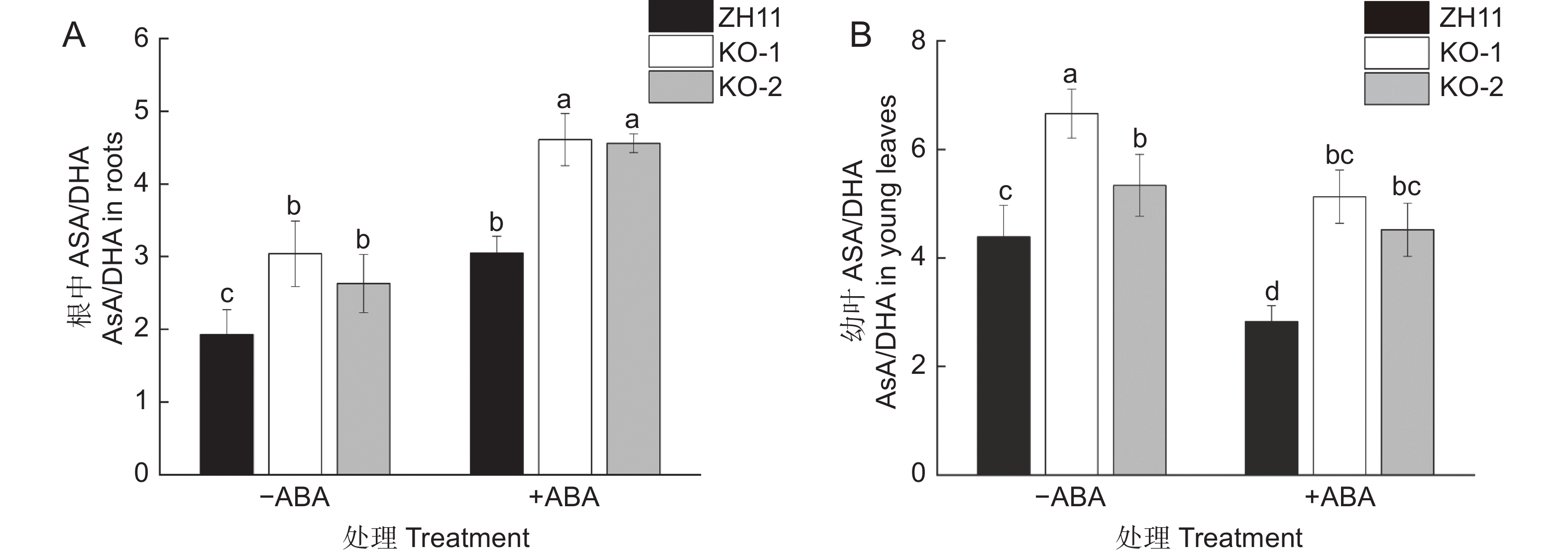
不论是野生型还是敲除系,ABA处理对其根的AsA/DHA比值影响不大(图6:A);但幼叶中的AsA/DHA比值在处理间差异明显。未经ABA处理下,野生型幼叶的AsA/DHA值为4.39,而KO-1和KO-2为6.66和5.34,分别为野生型的1.51倍和1.22倍。ABA处理后,野生型幼叶AsA/DHA的值降低至2.83,KO-1和KO-2则分别降低至5.13和4.52,为野生型的1.81倍和1.6倍(图6:B),表明OsAAO4的敲除导致了AsA/DHA值的升高。
2.6 GO和KEGG富集分析
本研究还对OsAAO4敲除系与野生型的差异表达基因进行了GO和KEGG富集分析,结果如附图1
1 )所示。在未经ABA处理下,野生型‘中花11’和敲除系KO-1幼叶的生物过程、细胞组分和分子功能的差异相对较少,生物进程主要富集刺激响应和非刺激响应,细胞组分主要富集叶绿体基质(Chloroplast stroma)和质粒基质(Plastid stroma),分子功能主要富集DNA结合转录因子(DNA-binding transcription factor activity)(附图1:A)。ABA处理9 h后,二者间的差异表达基因明显增加,富集于16种不同类型的生物过程、4种不同的细胞组分和10种不同的分子功能。其中,生物过程显著富集氧化还原过程(Oxidation-reduction process)和氧化应激反应(Response to oxidative treatment),细胞组分显著富集光系统途径(Photosystem),分子功能显著富集催化作用途径(Catalytic activity)(附图1:B)。KEGG富集分析发现,未经ABA处理时,野生型和敲除系KO-1幼叶的代谢差异富集于次级代谢物生物合成(Biosynthesis of secondary metabolites)、氨基酸生物合成(Biosynthesis of amino acids)和光合生物的碳固定(Carbon fixation in photosynthetic organisms)等20条途径,以次级代谢物的生物合成居多。在ABA处理下,其功能途径的差异基因主要富集在基础代谢物(Metabolic pathways)、次级代谢物(Biosynthesis of secondary metabolites)和甘油磷脂代谢(Glycerophospholipid metabolism)等20条途径(附图1:C)。值得注意的是,敲除系在ABA处理下抗坏血酸相关基因表达上调,而光合作用-天线蛋白差异基因的表达水平下调(附图1:D)。
3. 讨论
细胞氧化还原状态由氧化系统和还原系统共同调控。氧化系统主要包括活性氧和活性氮(RNS),还原系统主要包括抗氧化物酶类(如谷胱甘肽还原酶、过氧化氢酶、谷胱甘肽过氧化物酶等)、抗氧化剂(如谷胱甘肽、抗坏血酸、维生素E等)以及硫氧还蛋白系统和谷氧还蛋白系统[16]。维持不同区隔化空间的氧化还原稳态对于细胞生命活动而言至关重要。质外体由细胞壁、细胞间隙和导管组成,是感受和应答环境信号的前沿区域[17]。在遭受环境胁迫后,质外体信号系统一方面将环境变化反馈至共质体,另一方面又作为细胞间的通讯工具长距离传递共质体信息[18]。利用质外体氧化还原系统实现信号转导并激活表达调控系统,对于提高植物的耐逆性具有重要意义。
ABA参与胞间与胞内逆境信号传导途径,通过调节细胞渗透压、气孔导度及诱导胁迫响应基因的表达来适应环境的变化[19]。ABA信号转导组分ABI3、ABI4、ABI5等转录因子结合响应基因启动子区域的ABRE,进而激活或抑制下游基因的表达,调节种子萌发、幼苗生长[20-23]。水稻AAO家族成员中,OsAAO1~OsAAO5均含有非生物胁迫相关元件(如干旱诱导的MYB结合位点、厌氧诱导元件),但OsAAO1、OsAAO4和OsAAO5不含脱落酸响应元件;OsAAO2和OsAAO4都携带有ABA响应元件,其中OsAAO4含有9个脱落酸响应元件。ABA处理9 h后,OsAAO4在根和幼叶中的表达量分别达到野生型的13.8倍和7.4倍,说明OsAAO4受ABA诱导表达。为进一步探讨OsAAO4的生物学功能,我们构建了2个OsAAO4敲除纯系。不论是正常条件还是ABA处理条件下,敲除系的AAO活性都低于野生型,证实了OsAAO4具有调节抗坏血酸氧化酶活性的能力。正常条件下,敲除系和野生型的生长势没有显著差异,但在ABA处理下,敲除系的存活率和株高均明显降低,且随着ABA处理浓度的升高降低加剧。这表明OsAAO4在调节逆境下幼苗的正常生长发育方面具有重要作用,但OsAAO4是否与ABI蛋白存在互作尚不清楚。
还原态和氧化态的抗坏血酸都是质外体氧化还原系统的重要组成部分,其动态平衡受抗坏血酸氧化酶的精确调控[24]。在烟草(Nicotiana tabacum L.)中,反义表达AAO植株的AsA含量升高,过氧化氢的清除能力增强,耐盐性提高[25];而过表达AAO植株的AsA含量下降,盐敏感性增强[7]。在水稻中,过表达AAO的负调控靶标miR528显著增加了AsA含量,抑制了ROS的积累,从而增强了植株耐盐性。相反,敲除miR528或过表达AAO则降低AsA的含量,促进ROS的积累,导致水稻耐盐性的下降[26]。
OsAAO4是调节质外体抗坏血酸氧化的重要工具。过表达DHAR提高还原态AsA的含量,增强植物对臭氧的耐受性,表明AsA的积累有利于提高植物的耐逆性[27]。在甜瓜(Cucumis melo L.)中,抑制AAO的表达,则抗坏血酸氧化受阻,AsA含量增加,导致生长变缓[28]。在水稻中,敲除OsAAO3或OsAAO4都可导致抵御稻瘟病菌侵染的能力减弱[11]。与此类似,敲除OsAAO4的植株中,尽管AsA的含量显著提高,但在ABA胁迫下幼苗的生长受到明显抑制,表明抗坏血酸氧化对植物抗病抗逆性具有积极作用。这些现象暗示质外体抗坏血酸的氧化态和还原态的改变可引发水稻不同的胁迫应答效应。
抗坏血酸氧化不仅能影响还原态抗坏血酸的含量,还能调节还原态与氧化态抗坏血酸的比例。在正常条件下,两个OsAAO4敲除系中幼叶的AsA/DHA值较野生型分别升高了1.51倍和1.22倍;ABA处理后,较野生型分别升高了1.81倍和1.60倍。质外体抗坏血酸稳态是确保信号系统正常工作的基础。在ABA处理下,OsAAO4敲除系和野生型幼叶的差异表达基因明显富集于氧化还原和氧化应激途径。抑制抗坏血酸氧化,可能会影响质外体pH感受器和细胞膜NADPH氧化酶(NOX)的活性[29],造成细胞内活性氧的积累,导致幼苗的生长受阻。本研究明确了OsAAO4介导的抗坏血酸氧化是维持逆境下水稻幼苗生长的生理基础,为深入认识抗坏血酸稳态的遗传调控网络及其生物学功能提供了新的视角。
1 如需查阅附图内容请登录《植物科学学报》网站(http://www.plantscience.cn)查看本期文章。 -
图 4 OsAAO4敲除系与野生型(ZH11)幼苗长势(A)、株高(B)与存活率(C)的比较
不同小写字母表示OsAAO4敲除系与野生型间差异显著(P<0.05)。下同。
Figure 4. Growth (A), plant height (B), and survival rate (C) of OsAAO4 knockout and wild-type lines under ABA treatment
Different lowercase letters indicate significant differences between OsAAO4 knockout lines and wild-type at 0.05 level. Same below.
-
[1] Rong L,Xin S,Tao CC,Jin X,Li HB. Cotton ascorbate oxidase promotes cell growth in cultured tobacco bright yellow-2 cells through generation of apoplast oxidation[J]. Int J Mol Sci,2017,18(7):1346 doi: 10.3390/ijms18071346
[2] Guo ZF,Tan HQ,Zhu ZH,Lu SY,Zhou BY. Effect of intermediates on ascorbic acid and oxalate biosynthesis of rice and in relation to its stress resistance[J]. Plant Physiol Biochem,2005,43(10-11):955−962. doi: 10.1016/j.plaphy.2005.08.007
[3] Smirnoff N,Wheeler GL. Ascorbic acid in plants:biosynthesis and function[J]. Crit Rev Biochem Mol Biol,2000,35(4):291−314. doi: 10.1080/10409230008984166
[4] Gallie DR. The role of L-ascorbic acid recycling in responding to environmental stress and in promoting plant growth[J]. J Exp Bot,2013,64(2):433−443. doi: 10.1093/jxb/ers330
[5] De Tullio MC,Liso R,Arrigoni O. Ascorbic acid oxidase:an enzyme in search of a role[J]. Biol Plantarum,2004,48(2):161−166. doi: 10.1023/B:BIOP.0000033439.34635.a6
[6] Pignocchi C,Fletcher JM,Wilkinson JE,Barnes JD,Foyer CH. The function of ascorbate oxidase in tobacco[J]. Plant Physiol,2003,132(3):1631−1641. doi: 10.1104/pp.103.022798
[7] Fotopoulos V,Sanmartin M,Kanellis AK. Effect of ascorbate oxidase over-expression on ascorbate recycling gene expression in response to agents imposing oxidative stress[J]. J Exp Bot,2006,57(14):3933−3943. doi: 10.1093/jxb/erl147
[8] Batth R,Singh K,Kumari S,Mustafiz A. Transcript profiling reveals the presence of abiotic stress and developmental stage specific ascorbate oxidase genes in plants[J]. Front Plant Sci,2017,8:198.
[9] Zechmann B. Subcellular distribution of ascorbate in plants[J]. Plant Signal Behav,2011,6(3):360−363. doi: 10.4161/psb.6.3.14342
[10] Ueda Y,Siddique S,Frei M. A novel gene,OZONE-RESPONSIVE APOPLASTIC PROTEIN1,enhances cell death in ozone stress in rice[J]. Plant Physiol,2015,169(1):873−889. doi: 10.1104/pp.15.00956
[11] Hu JX,Liu MX,Zhang A,Dai Y,Chen WZ,et al. Co-evolved plant and blast fungus ascorbate oxidases orchestrate the redox state of host apoplast to modulate rice immunity[J]. Mol Plant,2022,15(8):1347−1366. doi: 10.1016/j.molp.2022.07.001
[12] Singh RR,Verstraeten B,Siddique S,Tegene AM,Tenhaken R,et al. Ascorbate oxidation activates systemic defence against root-knot nematode Meloidogyne graminicola in rice[J]. J Exp Bot,2020,71(14):4271−4284. doi: 10.1093/jxb/eraa171
[13] 童超. ABA生理功能与信号转导相关综述[J]. 科技资讯,2008(10):44−45. doi: 10.3969/j.issn.1672-3791.2008.10.037 [14] Teng KQ,Li JZ,Liu L,Han YC,Du YX,et al. Exogenous ABA induces drought tolerance in upland rice:the role of chloroplast and ABA biosynthesis-related gene expression on photosystem Ⅱ during PEG stress[J]. Acta Physiol Plant,2014,36(8):2219−2227. doi: 10.1007/s11738-014-1599-4
[15] Sanmartin M,Pateraki I,Chatzopoulou F,Kanellis AK. Differential expression of the ascorbate oxidase multigene family during fruit development and in response to stress[J]. Planta,2007,225(4):873−885. doi: 10.1007/s00425-006-0399-5
[16] Postiglione AE,Muday GK. The role of ROS homeostasis in ABA-induced guard cell signaling[J]. Front Plant Sci,2020,11:968. doi: 10.3389/fpls.2020.00968
[17] Farvardin A,González-Hernández AI,Llorens E,García-Agustín P,Scalschi L,et al. The apoplast:a key player in plant survival[J]. Antioxidants,2020,9(7):604. doi: 10.3390/antiox9070604
[18] Rogalla H,Römheld V. Role of leaf apoplast in silicon-mediated manganese tolerance of Cucumis sativus L.[J]. Plant Cell Environ,2002,25(4):549−555. doi: 10.1046/j.1365-3040.2002.00835.x
[19] Li JJ,Li Y,Yin ZG,Jiang JH,Zhang MH,et al. OsASR5 enhances drought tolerance through a stomatal closure pathway associated with ABA and H2O2 signalling in rice[J]. Plant Biotechnol J,2017,15(2):183−196.
[20] Söderman EM,Brocard IM,Lynch TJ,Finkelstein RR. Regulation and function of the Arabidopsis ABA-insensitive4 gene in seed and abscisic acid response signaling networks[J]. Plant Physiol,2000,124(4):1752−1765. doi: 10.1104/pp.124.4.1752
[21] Finkelstein RR,Lynch TJ. The Arabidopsis abscisic acid response gene ABI5 encodes a basic leucine zipper transcription factor[J]. Plant Cell,2000,12(4):599−609. doi: 10.1105/tpc.12.4.599
[22] Finkelstein RR,Somerville CR. Three classes of abscisic acid (ABA)-insensitive mutations of Arabidopsis define genes that control overlapping subsets of ABA responses[J]. Plant Physiol,1990,94(3):1172−1179. doi: 10.1104/pp.94.3.1172
[23] Yang C,Li XB,Chen SQ,Liu CL,Yang LM,et al. ABI5-FLZ13 module transcriptionally represses growth-related genes to delay seed germination in response to ABA[J]. Plant Commun,2023,4(6):100636. doi: 10.1016/j.xplc.2023.100636
[24] Liso R,De Tullio MC,Ciraci S,Balestrini R,La Rocca N,et al. Localization of ascorbic acid,ascorbic acid oxidase,and glutathione in roots of Cucurbita maxima L.[J]. J Exp Bot,2004,55(408):2589−2597. doi: 10.1093/jxb/erh262
[25] Yamamoto A,Bhuiyan NH,Waditee R,Tanaka Y,Esaka M,et al. Suppressed expression of the apoplastic ascorbate oxidase gene increases salt tolerance in tobacco and Arabidopsis plants[J]. J Exp Bot,2005,56(417):1785−1796. doi: 10.1093/jxb/eri167
[26] Wang M,Guo WP,Li J,Pan XJ,Pan LH,et al. The miR528-AO module confers enhanced salt tolerance in rice by modulating the ascorbic acid and abscisic acid metabolism and ROS scavenging[J]. J Agric Food Chem,2021,69(31):8634−8648. doi: 10.1021/acs.jafc.1c01096
[27] Chen Z,Gallie DR. Increasing tolerance to ozone by elevating foliar ascorbic acid confers greater protection against ozone than increasing avoidance[J]. Plant Physiol,2005,138(3):1673−1689. doi: 10.1104/pp.105.062000
[28] Chatzopoulou F,Sanmartin M,Mellidou I,Pateraki I,Koukounaras A,et al. Silencing of ascorbate oxidase results in reduced growth,altered ascorbic acid levels and ripening pattern in melon fruit[J]. Plant Physiol Biochem,2020,156:291−303. doi: 10.1016/j.plaphy.2020.08.040
[29] Wang GF,Li WQ,Li WY,Wu GL,Zhou CY,et al. Characterization of rice NADPH oxidase genes and their expression under various environmental conditions[J]. Int J Mol Sci,2013,14(5):9440−9458. doi: 10.3390/ijms14059440
-
其他相关附件
-
PDF格式
孙林娟 附图 1 点击下载(466KB)
-



 下载:
下载: