Effect of sex and leaf shape on gas exchange parameters and chlorophyll fluorescence characteristics in Sabina chinensis (L.) Ant
-
摘要:
为分析性别及叶形对光合能力、能量分配与耗散的影响,本研究以圆柏(Sabina chinensis (L.) Ant.)雌株、雄株和雌雄同株3种个体的鳞叶和刺叶为材料,测定了气体交换参数、叶绿素荧光特性参数和非结构性碳水化合物(NSC)的含量。结果显示:雌株和雄株刺叶的净光合速率(Pn)、蒸腾速率(Tr)、气孔导度(Gs)、水分利用率(WUE)和NSC显著高于鳞叶;雄株、雌株刺叶的非光化光淬灭系数(NPQ)和光能捕获能力(1/Fo−1/Fm)显著高于鳞叶,最大光化学量子效率(Fv/Fm)、实际电子传递速率(ETR)、实际光化学量子效率(ФPSⅡ)、光化光淬灭系数(qP)、潜在最大电子传递速率(rETRmax)和半饱和光强(Ik)显著低于鳞叶。雌株的Pn、NSC、NPQ和1/Fo−1/Fm显著高于雄株, Fv/Fm、ETR、qP、rETRmax和Ik显著低于雄株。相关性分析表明,NSC与Pn和1/Fo−1/Fm呈极显著正相关,与ETR呈显著负相关。研究结果表明,圆柏刺叶通过提高光能捕获能力及热散耗能力适应强光照环境,而鳞叶通过提高光能利用效率和光保护机制,能够适应弱光照环境。雌株可通过较强的光合速率获取较多的NSC,从而满足其生长繁殖的需求。
Abstract:This study investigated the effects of sex and leaf morphology on photosynthetic capacity, energy allocation, and dissipation in Sabina chinensis (L.) Ant. The experimental materials included prickly and scaly leaves from female, male, and monoecious plants. Gas exchange parameters, chlorophyll fluorescence characteristics, and non-structural carbohydrate (NSC) content were measured. Results showed that prickly leaves from both female and male plants exhibited significantly higher photosynthetic rate (Pn), the transpiration rate (Tr), the stomatal conductance (Gs), water use efficiency (WUE), and NSC compared to scaly leaves. Similarly, the non-photochemical quench (NPQ) and the ability of PSⅡ reaction center to trap energy from antenna pigment (1/Fo−1/Fm) were significantly higher in male and female prickly leaves, while maximum photochemical efficiency (Fv/Fm), the electron transfer rate (ETR), actual photochemical quantum efficiency (ФPSⅡ), photochemical quenching (qP), the highest maximum relative electron transfer rate (rETRmax), and half-saturated light intensity (Ik) were significantly lower in male and female prickly leaves compared to scaly leaves. Among sexes, female plants demonstrated significantly higher Pn, NSC, NPQ, and 1/Fo−1/Fm than male plants, while Fv/Fm, ETR, qP, rETRmax, and Ik were significantly lower in females. Correlation analysis showed a strong positive correlation between NSC and both Pn and 1/Fo−1/Fm, but a strong negative correlation between NSC and ETR. In conclusion, prickly leaves adapt to high-light environments by improving light energy capture ability and heat dissipation ability, whereas scaly leaves adapt to low-light environments by improving light energy utilization efficiency and light protection mechanisms. The coexistence of prickly and scaly leaves allows S. chinensis to meet the demands for photosynthate production and adapt to varying light conditions during growth and development. Female plants, through higher Pn, achieve greater NSC content, supporting the requirements for reproduction and growth.
-
光合作用作为地球上最重要的一个生理生化过程,为植物生长发育提供了大部分物质和能量[1]。叶片是绿色植物吸收光能和形成同化力的光合器官,植物生长季,其光合机构面临既需要光能又要避免强光、高温等胁迫伤害的情况[2]。因此,一些物种在长期进化过程中形成的异形叶机制,在适应环境方面发挥着重要作用[3, 4]。柏科许多物种均有明显的异形叶[5],而关于柏科的鳞叶和刺叶光合功能差异的研究较少,主要集中于圆柏属(Sabina)物种。臭柏(Juniperus sabina L.)鳞叶单位面积的光合速率高于刺叶,对强光引起的光抑制有更好的耐性;刺叶单位鲜重的光合速率高于鳞叶,且刺叶光补偿点更低[6]。但也有研究结果与之相反,认为臭柏刺叶单位面积的光合速率和水分利用效率高于鳞叶[7, 8]。球柏(J. chinensis 'Globosa')刺叶的净光合速率高于鳞叶[9]。因此,关于圆柏属刺叶和鳞叶的光合能力差异尚存在争议。
雌雄异株是物种对环境长期适应的进化结果[10],雌雄株在生长发育、生理特性、空间分布和资源配置等方面有明显的性别差异[11]。在雌雄异株树木的性别响应差异方面,针对光合特征的研究主要集中在对干旱、极端温度、盐、养分和重金属等非生物因子以及竞争等生物因子的应答能力[12]。雌、雄株对胁迫的反应并不相同[13-16]。以温室盆栽幼苗为材料时,一些物种雌株的光合参数数值高于雄株[16, 17],或低于雄株[14, 15],抑或两者相似[13, 18],这些结果可能源于幼苗与成龄树之间的差异[19]。在自然条件下,雌雄异株成年树间的光合差异明显稳定,除刺柏槲寄生(Phoradendron juniperinum Engelm.)[20]外,北极柳[21](Salix arctica Pall.)、梣叶槭[22]( Acer negundo L.)、窄叶杨[23](Populus angustifolia E. James)、杞柳[24] (S. integra Thunb. in Murray)、连香树[25] (Cercidiphyllum japonicum Siebold & Zucc.)、鼠李[26] (Rhamnus davurica Pall. )等雌株的气体交换参数值均高于雄株。
圆柏(S. chinensis (L.) Ant.)为圆柏属常绿植物,该物种雌雄异株,稀同株,具有鳞叶和刺叶两种叶形。圆柏在我国分布广泛,是北方重要的园林树种。目前,有关圆柏生理代谢的研究主要集中在刺叶的生理抗性[27, 28]、挥发性物质[29]、鳞叶的气孔特征[30]以及刺叶光合日变化[31]等方面,有关性别和叶形对气体交换参数和叶绿素荧光特征的影响报道较少。为此,本研究以圆柏雌株、雄株和雌雄同株的鳞叶和刺叶为材料,对气体交换参数、叶绿素荧光参数和非结构性碳水化合物(NSC)含量进行测定,以期揭示性别和叶形对圆柏光合生理功能的影响,探讨其对光照的适应机制,为圆柏的进化机制研究提供基础。
1. 材料与方法
1.1 研究区概况
样树生长于山西省晋中市太谷区山西农业大学(37°42′N,112°58′E),该地区海拔870 m,属于暖温带大陆气候,年平均气温为9.8 ℃,年平均降水量为456 mm,年均蒸发量为1 740 mm,无霜期年均176 d。
1.2 样树选择
选择生境一致的圆柏样树,雌株、雄株、雌雄同株各3株,样树为同批次栽植,树龄相同,树高和胸径相似,平均胸径为(12.1±0.8)cm。分别选择圆柏树体中部位置的东、南、西3个向阳方位的外围枝条,各方位的鳞、刺叶分别测试3次。
1.3 测定方法
1.3.1 气体交换参数测定
2023年8月,在晴朗无风天气下,基于相同面积,使用Ci-340便携式光合作用测定仪进行气体交换参数测定,测定时间为8:00-18:00,每间隔2 h测定1次,重复3次。指标为:净光合速率(Pn)、蒸腾速率(Tr)、胞间CO2浓度(Ci)、气孔导度(Gs),水分利用率(WUE=Pn/Tr)由公式计算得来。
1.3.2 叶绿素荧光参数测定
叶绿素荧光参数测定前,叶片经过夜间充分暗适应,于次日凌晨4:00-5:00,使用便携式调制叶绿素荧光仪PAM-2500测定PSⅡ实际光化学量子效率(ФPSⅡ)、实际电子传递速率(ETR)、光化光淬灭系数(qP)、非光化光淬灭系数(NPQ)、最小初始荧光(Fo)和最大荧光(Fm),并由仪器自动计算暗适应下PSⅡ最大光化学量子效率(Fv/Fm),最后,计算光能捕获能力(1/Fo−1/Fm)。
1.3.3 快速光响应曲线(RLC)的测量与分析
光合有效辐射(PAR)梯度依次为:0、55、77、144、257、332、430、940、1 364、1 981 μmol·m−2·s−1,持续时间为20 s,测定相对电子传递速率(Relative electron transport rate,rETR),参照Ralph和Gademann[32]的方法,拟合快速光响应曲线,得到光能利用效率(α)、潜在最大电子传递速率(rETRmax)和半饱和光强(Ik)。
1.3.4 非结构性碳水化合物含量测定
非结构性碳水化合物含量的测定采用硫酸蒽酮法[33],测定叶中的可溶性糖(SS)和淀粉(ST)含量。NSC含量为SS与ST含量之和。
1.4 数据处理
所有数据均以平均值±标准误(Mean±SD)表示。使用SPSS 18.0软件进行单因素方差分析和Pearson相关系数分析,P<0.05为差异显著,P<0.01为差异极显著。使用Excel 2019和Origin 2018软件绘制图形。
2. 结果与分析
2.1 气体交换参数比较
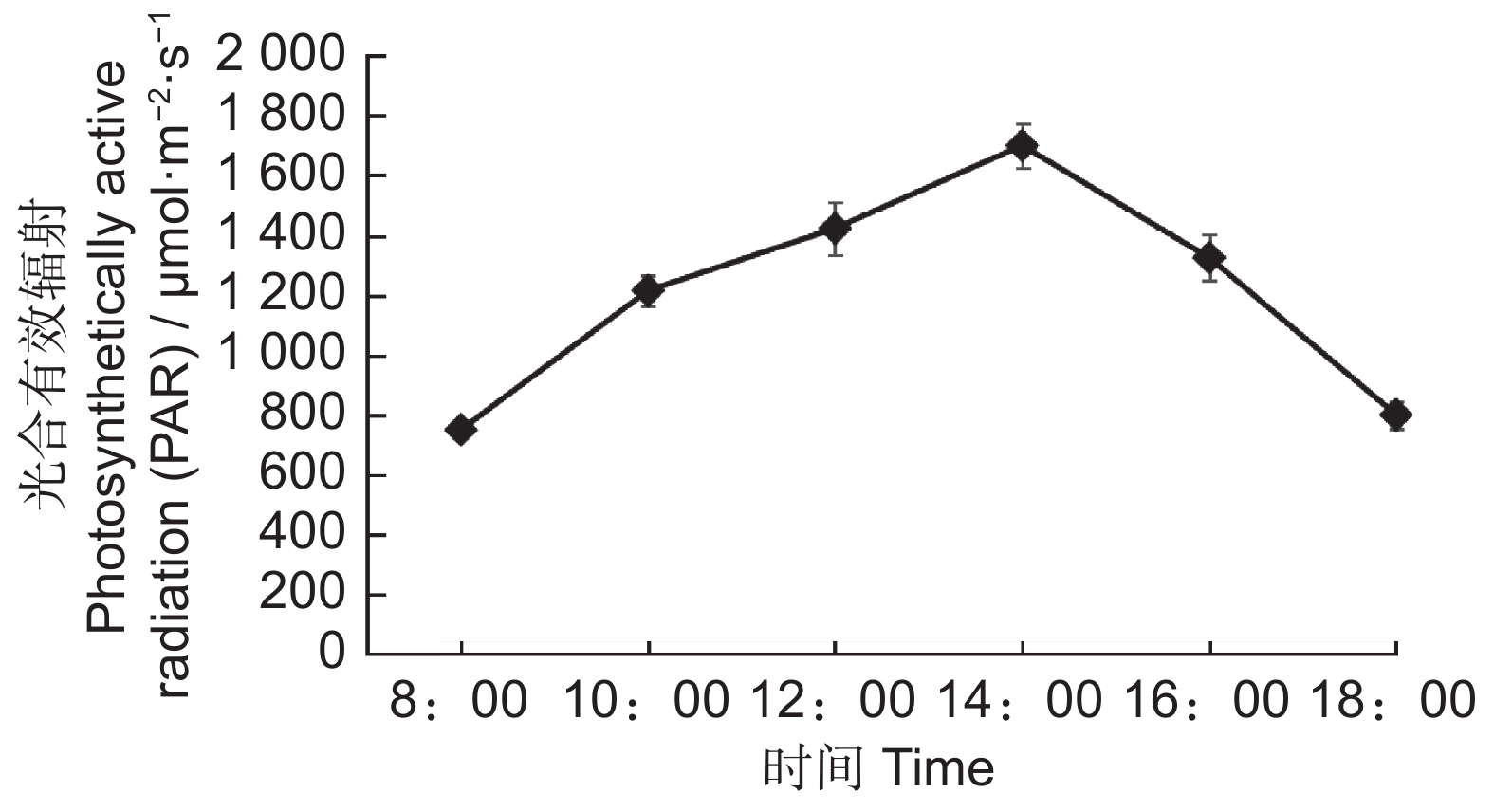
由图1可知,晴天时圆柏光合有效辐射的日变化呈单峰曲线,在14:00达到峰值,日均值为1 202 μmol·m-2·s-1。由表1可知,雌株、雄株、雌雄同株的刺叶和鳞叶Pn日变化呈双峰曲线。“午休”现象出现在14:00,第1峰值均出现在10:00,第2峰值在16:00,第2峰值显著低于第1峰值。在刺叶方面,雌株Pn最高,雌雄同株Pn最低。在鳞叶方面,雌株Pn最高,雄株Pn最低。另外,3种性别植株的刺叶和鳞叶的最大Pn峰值出现时间均早于PAR峰值4小时,二者变化不同步。在14:00时,光合作用受到光抑制,雄株的鳞叶受光抑制程度最严重,与10:00时相比,雄株的刺叶Pn下降了89.40%,鳞叶Pn下降了92.13%。而雌株刺叶和鳞叶的Pn分别下降了86.44% 和81.07%。
表 1 4种光合参数的日变化Table 1. Comparison of four photosynthetic parameters参数
Parameter性别
Sex叶形
Leaf
shape时间
Time8:00 10:00 12:00 14:00 16:00 18:00 Pn / μmol·
m−2·s−1雄株 刺叶 1.2±0.10b(A) 3.5±0.10b(A) 1.7±0.10b(A) 0.4±0.02b(A) 0.9±0.20b(A) 0.1±0.10c(B) 鳞叶 0.7±0.05B(B) 2.2±0.30A(B) 1.2±0.10B(B) 0.2±0.03B(B) 0.7±0.04C(A) 0.3±0.03B(A) 雌株 刺叶 2.2±0.15a(A) 4.7±0.30a(A) 2.9±0.23a(A) 0.6±0.06a(A) 2.8±0.30a(A) 0.9±0.05a(A) 鳞叶 0.8±0.08B(B) 2.8±0.34A(B) 1.4±0.07A(B) 0.5±0.01A(B) 1.3±0.13B(B) 0.3±0.03C(B) 雌雄
同株刺叶 0.7±0.04c(B) 1.8±0.21c(B) 0.5±0.05c(B) 0.2±0.08c(B) 0.9±0.17b(B) 0.3±0.01b(B) 鳞叶 1.2±0.12A(A) 2.7±0.21A(A) 0.9±0.08C(A) 0.6±0.06A(A) 1.5±0.12A(A) 0.8±0.02A(A) Gs / mmol·
m−2·s−1雄株 刺叶 18.0±0.80a(A) 25.6±2.20a(A) 19.7±1.20b(A) 25.7±1.50a(A) 15.3±1.00b(A) 10.1±0.70a(B) 鳞叶 15.0±0.90A(B) 25.9±1.70A(A) 11.5±2.40B(B) 19.1±2.10A(B) 15.6±2.10A(A) 14.2±0.80A(A) 雌株 刺叶 19.1±1.10a(A) 22.1±1.80a(A) 24.4±1.50a(A) 17.5±1.20b(A) 29.9±1.10a(A) 10.8±0.70a(A) 鳞叶 15.3±1.00A(B) 23.1±1.40A(A) 21.1±2.10A(A) 17.7±1.20A(A) 17.8±1.50A(B) 9.8±0.99B(A) 雌雄
同株刺叶 14.0±0.90b(A) 20.1±2.10a(A) 17.0±1.60b(B) 15.0±1.30b(B) 18.0±1.80b(A) 9.9±0.56a(A) 鳞叶 14.0±0.90A(A) 23.1±3.00A(A) 23.0±1.40A(A) 21.0±1.90A(A) 19.0±1.40A(A) 11.0±0.90B(A) Tr / mmol·
m−2·s−1雄株 刺叶 0.4±0.02a(A) 1.1±0.03a(B) 1.4±0.05a(A) 1.7±0.08a(A) 0.9±0.08b(A) 0.4±0.03a(B) 鳞叶 0.3±0.05A(B) 1.2±0.06A(A) 0.8±0.04B(B) 1.0±0.03C(B) 0.7±0.04A(B) 0.7±0.09A(A) 雌株 刺叶 0.4±0.15a(A) 0.7±0.07c(A) 0.8±0.12b(B) 1.3±0.06b(B) 1.1±0.09a(A) 0.3±0.05b(B) 鳞叶 0.3±0.08A(A) 0.9±0.14B(A) 1.0±0.07A(A) 1.4±0.01A(A) 0.8±0.13A(B) 0.4±0.03B(A) 雌雄
同株刺叶 0.2±0.04b(A) 0.9±0.11b(A) 0.6±0.05c(B) 1.0±0.08c(B) 0.8±0.07b(A) 0.3±0.01b(A) 鳞叶 0.3±0.12A(A) 0.7±0.09B(A) 0.8±0.08B(A) 1.3±0.06B(A) 0.8±0.12A(A) 0.3±0.02C(A) WUE /
mmol/
mol雄株 刺叶 3.0±0.10c(A) 2.7±0.18b(A) 0.7±0.10b(B) 0.2±0.04b(A) 1.0±0.20b(A) 0.3±0.10c(B) 鳞叶 2.3±0.05C(B) 1.6±0.30C(B) 0.9±0.10A(A) 0.2±0.02B(A) 1.0±0.04C(A) 0.5±0.03B(A) 雌株 刺叶 5.5±0.15a(A) 5.3±0.30a(A) 3.5±0.23a(A) 0.5±0.06a(A) 2.5±0.30a(A) 2.7±0.05a(A) 鳞叶 2.7±0.18B(B) 2.6±0.34B(B) 1.4±0.27A(B) 0.4±0.11A(B) 1.8±0.13B(B) 0.7±0.17B(B) 雌雄
同株刺叶l 3.3±0.04b(B) 2.0±0.21c(B) 0.8±0.05b(B) 0.2±0.08b(B) 1.2±0.17b(B) 1.1±0.01b(B) 鳞叶 3.9±0.12A(A) 3.7±0.24A(A) 1.1±0.18A(A) 0.4±0.12A(A) 2.0±0.12A(A) 2.5±0.13A(A) 注:不同小写字母表示同一参数下刺叶3种性别间差异显著,不同大写字母表示同一参数下鳞叶3种性别间差异显著,括号内不同大写字母表示同一参数下各性别鳞、刺叶间差异显著(P<0.05)。 Notes: Different lowercase letters indicate significant differences between sexes of prickly leaves under the same parameter, different uppercase letters indicate significant differences between sexes of scaly leaves under the same parameter, and different uppercase letters in parentheses indicate significant differences between sexes of scaly and prickly leaves under the same parameter (P<0.05). 由表1可见, 就刺叶的Pn和Gs来说,雌株Pn显著高于雄株和雌雄同株,雌株与雄株的Gs差异不显著。而鳞叶的Pn和Gs变化较复杂,雌株在8:00、10:00时与雄株无差异,在12:00、2:00、4:00时则显著高于雄株。Gs在雌株与雄株间无显著差异。就Tr和WUE而言,雄株和雌株的刺叶的Tr在8:00-14:00上升,之后下降;雌雄同株个体呈现两个峰值,分别出现在10:00和14:00。雄株的Tr在14:00-18:00始终高于雌雄同株个体,而雌株在该时间段高于雄株。鳞叶的Tr变化较为复杂,但雌株的WUE始终高于雄株,在8:00-10:00和14:00-18:00时,雌雄同株个体的WUE显著高于雌株,在12:00-14:00时,两者无显著差异。
比较鳞、刺叶的气体交换参数,发现对于Pn而言,8:00-16:00时雄株刺叶显著高于鳞叶,8:00-10:00时升高,然后持续下降到14:00,之后再次上升。在17:00时,刺叶的下降幅度较大,而鳞叶的下降速度较缓。在雌株中,8:00-18:00时刺叶显著高于鳞叶。在雌雄同株个体中,鳞叶显著高于刺叶,两者的变化趋势一致,且变化幅度较为平稳。对于Gs而言,雄株和雌株的变化趋势与Pn相同。在雄株中,刺叶在8:00-10:00升高,10:00-12:00下降;鳞叶在10:00达到顶峰,12:00-14:00再次升高后下降。在8:00、12:00-14:00,刺叶显著高于鳞叶。在雌株中,刺叶在8:00-12:00持续上升,12:00达到顶峰,鳞叶在10:00达到顶峰。刺叶在16:00达到第2个峰值,之后明显高于鳞叶。在雌雄同株个体中,8:00-18:00,刺叶和鳞叶间无显著差异。对于Tr而言,在雄株的刺叶中从8:00-14:00持续上升,之后下降。鳞叶在8:00-10:00期间先升高后下降,在14:00再次出现峰值。在8:00、12:00-16:00时,刺叶明显高于鳞叶。在雌株中,刺叶和鳞叶都在14:00达到峰值,12:00之前,鳞叶与刺叶的蒸腾速率无显著差异。12:00-14:00鳞叶显著高于刺叶,14:00之后,刺叶高于鳞叶。在雌雄同株个体中,变化曲线与雄株一致,但叶形相反。3种叶形的WUE变化趋势与“午休”时间一致,在14:00时最低。在雄株中,刺叶在12:00之前高于鳞叶,之后两者无显著差异。在雌株中,刺叶的WUE始终高于鳞叶。而在雌雄同株个体中,鳞叶的WUE始终高于刺叶。
2.2 叶绿素荧光参数差异
对比圆柏雌株、雄株和雌雄同株个体刺叶中的6种叶绿素荧光参数(表2),结果表明,Fv/Fm、ФPSⅡ在性别间无显著差异。ETR在雄株中显著高于雌株,雌雄同株与雄株无差异。NPQ在雌、雄株间无显著差异,雌株显著高于雌雄同株。就1/Fo−1/Fm而言,雌雄同株>雌株>雄株(P<0.05)。
表 2 不同性别圆柏异形叶叶绿素荧光参数Table 2. Chlorophyll fluorescence parameters of heterophyllous leaves of different sexes in Sabina chinensis叶形
Leaf shape性别
Sex最大光化光效率
Fv/Fm实际电子传递速率
ETR实际光化光效率
ФPSⅡ光化学淬灭系数
qP非光化学淬灭系数
NPQ光能捕获能力
1/Fo−1/Fm刺叶 雄株 0.78±0.014b 23.60±1.248c 0.22±0.011b 0.41±0.014b 1.96±0.165a 1.71±0.145c 雌株 0.78±0.013b 21.36±1.700d 0.20±0.016b 0.37±0.015c 2.12±0.126a 1.97±0.169b 雌雄同株 0.78±0.009b 24.65±0.150c 0.23±0.001b 0.41±0.003b 1.82±0.180ab 2.35±0.198a 鳞叶 雄株 0.81±0.010a 30.44±3.440a 0.28±0.046a 0.47±0.021a 1.63±0.129b 1.58±0.164d 雌株 0.78±0.011b 27.56±1.190b 0.26±0.030ab 0.44±0.020ab 2.01±0.141a 1.63±0.092cd 雌雄同株 0.80±0.002a 24.25±0.530c 0.22±0.039b 0.42±0.036b 2.07±0.113a 2.21±0.204a 注:同列不同小写字母表示差异显著(P<0.05)。 Note: Different lowercase letters in the same column indicate significant difference (P<0.05). 比较不同性别植株鳞叶中的6种叶绿素荧光参数,结果表明qP、ФPSⅡ在性别间无显著差异。雄株的Fv/Fm显著高于雌株,雄株与雌雄同株无差异。雌株的NPQ显著高于雄株,雌株与雌雄同株个体间无差异。对于1/Fo−1/Fm而言,雌株与雄株无差异,雌株显著高于雌雄同株个体。对于ETR而言,雄株>雌株>雌雄同株个体(P<0.05)。
比较不同性别个体鳞叶和刺叶的6种叶绿素荧光参数,结果发现,雄株中,鳞叶的Fv/Fm、ETR、ФPSⅡ、qP显著高于刺叶,而刺叶的NPQ、1/Fo−1/Fm显著高于鳞叶。雌株中,鳞叶的Fv/Fm、ФPSⅡ、NPQ与刺叶无显著差异,ETR、qP显著高于刺叶,而刺叶的1/Fo−1/Fm显著高于鳞叶。雌雄同株个体中,除鳞叶的Fv/Fm显著高于刺叶(P<0.05)外,其他荧光参数在两种叶形间无显著差异。
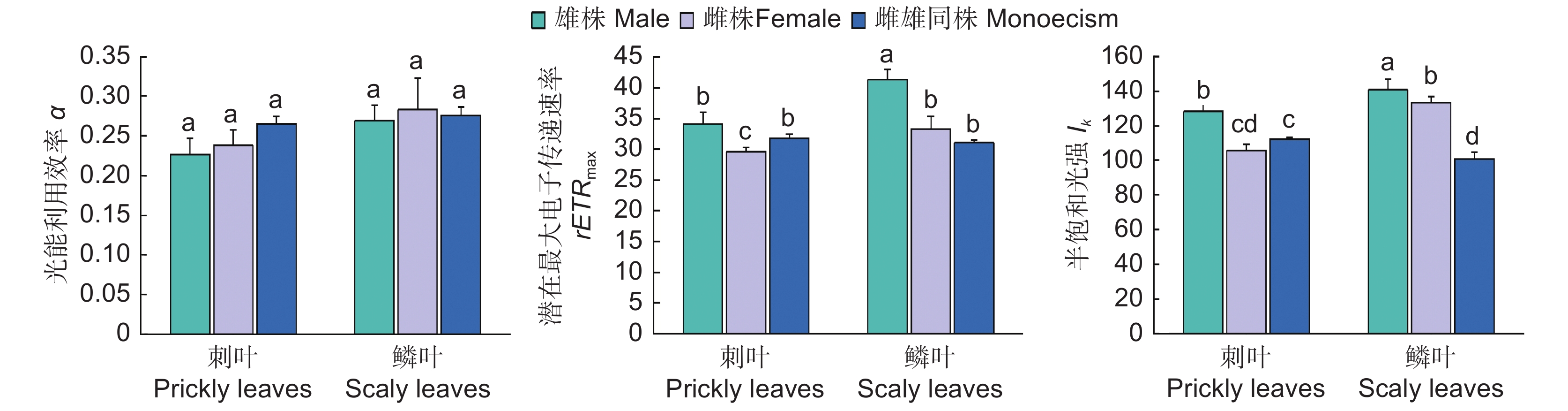
对刺叶α而言,雌雄同株个体>雌株>雄株;对鳞叶α而言,雌株>雌雄同株个体>雄株,但差异均不显著。对3种性别的植株而言,其α均表现为鳞叶>刺叶,但差异不显著(图2)。
在rETRmax方面,对刺叶而言,雄株显著高于雌株,雄株与雌雄同株个体无显著差异;对鳞叶而言,雄株显著高于雌株,雌株与雌雄同株个体无显著差异。比较两种叶形的差异,雄株和雌株均表现为鳞叶>刺叶(P<0.05)(图2)。
在Ik方面,对刺叶而言,雄株显著高于雌株,雌株与雌雄同株个体无差异;对鳞叶而言,表现为雄株>雌株>雌雄同株。比较两种叶形,雄株和雌株均表现为鳞叶>刺叶,雌雄同株个体则表现为刺叶>鳞叶(P<0.05)(图2)。
2.3 非结构性碳水化合物含量比较
由表3可知,3种性别的圆柏,其NSC含量在鳞叶与刺叶间均有显著差异。雌株和雄株中刺叶>鳞叶,雌雄同株个体中鳞叶>刺叶。对比刺叶NSC含量,发现雌株>雄株>雌雄同株,差异显著;分析鳞叶NSC含量,结果显示雌株显著高于雄株(P<0.05),雄株与雌雄同株个体无显著差异。
表 3 不同叶片非结构性碳水化合物含量Table 3. Non-structural carbohydrate content in different leaves性别
Sex叶形
Leaf shape可溶性糖
SS / mg/g淀粉
ST / mg/g非结构性碳水化合物
NSC / mg/g雄株 刺叶 66.33±3.17aB 23.76±1.93aA 90.09±5.10aB 鳞叶 69.20±3.37aA 14.67±2.53bB 83.87±5.90bB 雌株 刺叶 74.58±2.65aA 24.92±2.06aA 99.50±4.71aA 鳞叶 65.70±3.62bAB 21.65±2.11bA 87.34±5.73bA 雌雄同株 刺叶 55.37±4.38aC 22.03±1.80aA 77.40±6.19aC 鳞叶 61.50±3.65bB 20.39±1.28aA 81.89±4.93bB 注:不同小写字母表示相同性别下不同叶形间存在显著差异;不同大写字母表示相同叶形下不同性别间存在显著差异, P<0.05。 Notes: Different lowercase letters indicate significant differences between different leaf shapes in the same sex; different capital letters indicate significant differences between different sexes with the same leaf shape, P<0.05. 雌株和雌雄同株个体的鳞叶SS含量显著高于刺叶,雄株中鳞叶与刺叶差异不明显。分析刺叶SS含量,发现雌株>雄株>雌雄同株,均呈显著差异。对比鳞叶SS含量,结果显示,雌株与雄株之间差异不显著,而雌株显著高于雌雄同株个体(P<0.05)。
雌株和雄株中,刺叶ST含量显著高于鳞叶,而雌雄同株个体无显著差异。刺叶ST含量在3种性别植株中无显著差异。鳞叶ST含量检测发现,雌株显著高于雄株(P<0.05),雌株和雌雄同株个体间无显著差异。
2.4 相关性分析
相关性分析结果显示,NSC与Pn和 1/Fo−1/Fm呈极显著正相关(P<0.01),与ETR呈显著负相关(P<0.05)。
3. 讨论
3.1 叶形对气体交换参数及叶绿素荧光参数的影响
研究显示,同一生境下,圆柏雌、雄株刺叶的光合能力强于鳞叶,刺叶比鳞叶具有更高的Pn、NPQ、1/Fo−1/Fm、Tr、Gs和WUE。其中,NPQ反映的是PSⅡ天线色素吸收的未能用于光合电子传递,而是以热的形式耗散掉的光能部分,这是植物为了避免光抑制和膜受到伤害,调整过剩能量耗散的一套适应机制[34]。NPQ高时可以有效避免刺叶的PSⅡ光损耗,适应强光。1/Fo−1/Fm代表叶片获取光能的能力[35]。刺叶的1/Fo−1/Fm高于鳞叶,表示刺叶能够吸收更多光能,为碳同化提供更多化学能[36]。通常,在相同的饱和PAR下,光合速率越高,植物的光利用效率就越高,在强光下将越不容易受到光胁迫[37]。刺叶较高的光合速率与其较大的气孔导度也有密切关系,气孔导度大有助于叶片的CO2供应[38],同时增强光能的吸收,提高光合作用。
鳞叶的ETR、ФPSⅡ、qP、α、rETRmax和Ik均比刺叶高。ФPSⅡ反映叶片用于光合电子传递的能量占所吸收光能的比例,同时也是光合作用光抑制的度量指标。高ФPSⅡ有利于提高植物的光能转化效率,为暗反应的碳同化积累更多的能量[39]。qP反映PSⅡ天线色素吸收的光能用于光化学电子传递的份额,以及转化成化学能的效率,代表PSⅡ反应中心的开放程度[40]。本研究中,鳞叶的ETR、ФPSⅡ和qP均比刺叶高,表明鳞叶的光能转化效率和PSⅡ反应中心开放程度高于刺叶。在同一光照条件下,PSⅡ反应中心开放程度高时能接受到更多的光量子,鳞叶的PSⅡ受体QA还原速率比刺叶高,具有更强的电子传递能力,使得鳞叶具有更高的PSⅡ光化学效率。鳞叶的α、rETRmax和Ik比刺叶高,与上述推论一致,进一步说明鳞叶的光能转化效率高于刺叶。圆柏幼年期时个体较小,叶片数量较少,总体蒸腾耗水量较小,此时叶片以刺叶为主,具有更高的光合作用,能合成更多的营养物质,从而促进幼苗快速生长。随着植株的生长,刺叶逐渐转变为鳞叶,其光能利用效率及光耐受能力提高,在冬季光照较弱时,可以有效地将光能转化为化学能,使植株能够稳定地进行生理代谢[9]。
NSC是光合作用的产物。树木在白天以NSC的形式储存过剩的光合产物,当夜晚停止光合作用后,植株利用该产物供给代谢[41]。本研究中,在雌、雄株中,刺叶的NSC含量显著高于鳞叶。相关性分析结果显示,NSC含量与Pn、1/Fo−1/Fm呈正相关,与ETR呈负相关,表明净光合速率与光能捕获能力越高,NSC含量越高,进一步说明更高的Pn和1/Fo−1/Fm能使刺叶生产出更多的NSC,以供给植物生长发育。
雌雄同株个体的异形叶在光合参数方面与雌、雄株的趋势相反,而在叶绿素荧光参数方面与雌、雄株的变化趋势相同。目前,有关雌雄同株个体的生理研究较少。Quevedo-Rojas等[42]发现,一些物种能够通过增强NPQ来适应强光照,而其他物种则通过增加ΦPSⅡ和ETR来适应。刺叶的NPQ较高,而鳞叶的ΦPSⅡ、ETR和qP较高,两种叶形同时存在,使圆柏具有适应强光照的能力。
3.2 性别对光合及叶绿素荧光参数的影响
本研究发现,两种叶形的雌株光合能力均强于雄株,表现为雌株的Pn、Tr、WUE、NPQ和1/Fo−1/Fm高于雄株, NSC含量显著高于雄株。而NSC含量与Pn和1/Fo−1/Fm均呈极显著正相关,进一步说明雌株比雄株具有更高的光能捕获能力及热耗散能力,能够生产更多的营养物质,满足其繁殖生长的需要。本研究结果与其他雌雄异株植物中的研究报道一致[25, 26],这可能与雌株获取资源的补偿机制有关。雌株繁殖投入较高,它们会在其他生活史特征上表现出权衡,如雌株叶片在营养或繁殖生长期可增强营养器官的生长和光合作用,以获得更多的可利用资源,这样既能满足繁殖的资源需求,又没有减弱营养生长的资源投入[43]。雄株适应光照的策略与雌株不同,其具有更高的光能转化效率,能够更有效地利用捕获到的光能。雌雄同株个体中,刺叶的叶绿素荧光参数值均高于雌株和雄株,但气体交换参数Pn和WUE低于雄株和雌株;鳞叶的光能捕获能力及NPQ均高于雌株和雄株,光能转化效率低于雌株和雄株,但气体交换参数Pn和WUE高于雌株和雄株。这可能是由于雌雄同株个体同时具有雌株和雄株性质所导致的。
综上所述,圆柏雌株通过较强的光合速率获取较高的非结构性碳水化合物含量,表明雌株更适应强光照;而雄株可通过提高光能转化效率,有效利用光能,更适应弱光照;雌雄同株个体则兼具雌株和雄株的光照利用特点。刺叶可通过较强的光能捕获能力获取更高的NSC含量,同时具有较高的热耗散能力,表明其更适应强光照;而鳞叶的光能利用效率更高,适应弱光照。圆柏兼具鳞叶、刺叶两种叶形,异形叶机制具有“两头下注”的环境适应策略,使得圆柏能够适应不同的光照条件。
-
表 1 4种光合参数的日变化
Table 1 Comparison of four photosynthetic parameters
参数
Parameter性别
Sex叶形
Leaf
shape时间
Time8:00 10:00 12:00 14:00 16:00 18:00 Pn / μmol·
m−2·s−1雄株 刺叶 1.2±0.10b(A) 3.5±0.10b(A) 1.7±0.10b(A) 0.4±0.02b(A) 0.9±0.20b(A) 0.1±0.10c(B) 鳞叶 0.7±0.05B(B) 2.2±0.30A(B) 1.2±0.10B(B) 0.2±0.03B(B) 0.7±0.04C(A) 0.3±0.03B(A) 雌株 刺叶 2.2±0.15a(A) 4.7±0.30a(A) 2.9±0.23a(A) 0.6±0.06a(A) 2.8±0.30a(A) 0.9±0.05a(A) 鳞叶 0.8±0.08B(B) 2.8±0.34A(B) 1.4±0.07A(B) 0.5±0.01A(B) 1.3±0.13B(B) 0.3±0.03C(B) 雌雄
同株刺叶 0.7±0.04c(B) 1.8±0.21c(B) 0.5±0.05c(B) 0.2±0.08c(B) 0.9±0.17b(B) 0.3±0.01b(B) 鳞叶 1.2±0.12A(A) 2.7±0.21A(A) 0.9±0.08C(A) 0.6±0.06A(A) 1.5±0.12A(A) 0.8±0.02A(A) Gs / mmol·
m−2·s−1雄株 刺叶 18.0±0.80a(A) 25.6±2.20a(A) 19.7±1.20b(A) 25.7±1.50a(A) 15.3±1.00b(A) 10.1±0.70a(B) 鳞叶 15.0±0.90A(B) 25.9±1.70A(A) 11.5±2.40B(B) 19.1±2.10A(B) 15.6±2.10A(A) 14.2±0.80A(A) 雌株 刺叶 19.1±1.10a(A) 22.1±1.80a(A) 24.4±1.50a(A) 17.5±1.20b(A) 29.9±1.10a(A) 10.8±0.70a(A) 鳞叶 15.3±1.00A(B) 23.1±1.40A(A) 21.1±2.10A(A) 17.7±1.20A(A) 17.8±1.50A(B) 9.8±0.99B(A) 雌雄
同株刺叶 14.0±0.90b(A) 20.1±2.10a(A) 17.0±1.60b(B) 15.0±1.30b(B) 18.0±1.80b(A) 9.9±0.56a(A) 鳞叶 14.0±0.90A(A) 23.1±3.00A(A) 23.0±1.40A(A) 21.0±1.90A(A) 19.0±1.40A(A) 11.0±0.90B(A) Tr / mmol·
m−2·s−1雄株 刺叶 0.4±0.02a(A) 1.1±0.03a(B) 1.4±0.05a(A) 1.7±0.08a(A) 0.9±0.08b(A) 0.4±0.03a(B) 鳞叶 0.3±0.05A(B) 1.2±0.06A(A) 0.8±0.04B(B) 1.0±0.03C(B) 0.7±0.04A(B) 0.7±0.09A(A) 雌株 刺叶 0.4±0.15a(A) 0.7±0.07c(A) 0.8±0.12b(B) 1.3±0.06b(B) 1.1±0.09a(A) 0.3±0.05b(B) 鳞叶 0.3±0.08A(A) 0.9±0.14B(A) 1.0±0.07A(A) 1.4±0.01A(A) 0.8±0.13A(B) 0.4±0.03B(A) 雌雄
同株刺叶 0.2±0.04b(A) 0.9±0.11b(A) 0.6±0.05c(B) 1.0±0.08c(B) 0.8±0.07b(A) 0.3±0.01b(A) 鳞叶 0.3±0.12A(A) 0.7±0.09B(A) 0.8±0.08B(A) 1.3±0.06B(A) 0.8±0.12A(A) 0.3±0.02C(A) WUE /
mmol/
mol雄株 刺叶 3.0±0.10c(A) 2.7±0.18b(A) 0.7±0.10b(B) 0.2±0.04b(A) 1.0±0.20b(A) 0.3±0.10c(B) 鳞叶 2.3±0.05C(B) 1.6±0.30C(B) 0.9±0.10A(A) 0.2±0.02B(A) 1.0±0.04C(A) 0.5±0.03B(A) 雌株 刺叶 5.5±0.15a(A) 5.3±0.30a(A) 3.5±0.23a(A) 0.5±0.06a(A) 2.5±0.30a(A) 2.7±0.05a(A) 鳞叶 2.7±0.18B(B) 2.6±0.34B(B) 1.4±0.27A(B) 0.4±0.11A(B) 1.8±0.13B(B) 0.7±0.17B(B) 雌雄
同株刺叶l 3.3±0.04b(B) 2.0±0.21c(B) 0.8±0.05b(B) 0.2±0.08b(B) 1.2±0.17b(B) 1.1±0.01b(B) 鳞叶 3.9±0.12A(A) 3.7±0.24A(A) 1.1±0.18A(A) 0.4±0.12A(A) 2.0±0.12A(A) 2.5±0.13A(A) 注:不同小写字母表示同一参数下刺叶3种性别间差异显著,不同大写字母表示同一参数下鳞叶3种性别间差异显著,括号内不同大写字母表示同一参数下各性别鳞、刺叶间差异显著(P<0.05)。 Notes: Different lowercase letters indicate significant differences between sexes of prickly leaves under the same parameter, different uppercase letters indicate significant differences between sexes of scaly leaves under the same parameter, and different uppercase letters in parentheses indicate significant differences between sexes of scaly and prickly leaves under the same parameter (P<0.05). 表 2 不同性别圆柏异形叶叶绿素荧光参数
Table 2 Chlorophyll fluorescence parameters of heterophyllous leaves of different sexes in Sabina chinensis
叶形
Leaf shape性别
Sex最大光化光效率
Fv/Fm实际电子传递速率
ETR实际光化光效率
ФPSⅡ光化学淬灭系数
qP非光化学淬灭系数
NPQ光能捕获能力
1/Fo−1/Fm刺叶 雄株 0.78±0.014b 23.60±1.248c 0.22±0.011b 0.41±0.014b 1.96±0.165a 1.71±0.145c 雌株 0.78±0.013b 21.36±1.700d 0.20±0.016b 0.37±0.015c 2.12±0.126a 1.97±0.169b 雌雄同株 0.78±0.009b 24.65±0.150c 0.23±0.001b 0.41±0.003b 1.82±0.180ab 2.35±0.198a 鳞叶 雄株 0.81±0.010a 30.44±3.440a 0.28±0.046a 0.47±0.021a 1.63±0.129b 1.58±0.164d 雌株 0.78±0.011b 27.56±1.190b 0.26±0.030ab 0.44±0.020ab 2.01±0.141a 1.63±0.092cd 雌雄同株 0.80±0.002a 24.25±0.530c 0.22±0.039b 0.42±0.036b 2.07±0.113a 2.21±0.204a 注:同列不同小写字母表示差异显著(P<0.05)。 Note: Different lowercase letters in the same column indicate significant difference (P<0.05). 表 3 不同叶片非结构性碳水化合物含量
Table 3 Non-structural carbohydrate content in different leaves
性别
Sex叶形
Leaf shape可溶性糖
SS / mg/g淀粉
ST / mg/g非结构性碳水化合物
NSC / mg/g雄株 刺叶 66.33±3.17aB 23.76±1.93aA 90.09±5.10aB 鳞叶 69.20±3.37aA 14.67±2.53bB 83.87±5.90bB 雌株 刺叶 74.58±2.65aA 24.92±2.06aA 99.50±4.71aA 鳞叶 65.70±3.62bAB 21.65±2.11bA 87.34±5.73bA 雌雄同株 刺叶 55.37±4.38aC 22.03±1.80aA 77.40±6.19aC 鳞叶 61.50±3.65bB 20.39±1.28aA 81.89±4.93bB 注:不同小写字母表示相同性别下不同叶形间存在显著差异;不同大写字母表示相同叶形下不同性别间存在显著差异, P<0.05。 Notes: Different lowercase letters indicate significant differences between different leaf shapes in the same sex; different capital letters indicate significant differences between different sexes with the same leaf shape, P<0.05. -
[1] 李理渊,李俊,同小娟,孟平,张劲松,张静茹. 黄河小浪底栓皮栎、刺槐叶片电子传递速率-光响应的模拟[J]. 植物生态学报,2018,42(10):1009−1021. doi: 10.17521/cjpe.2018.0063 Li LY,Li J,Tong XJ,Meng P,Zhang JS,Zhang JR. Simulation on the light-response curves of electron transport rate of Quercus variabilis and Robinia pseudoacacia leaves in the Xiaolangdi area,China[J]. Chinese Journal of Plant Ecology,2018,42(10):1009−1021. doi: 10.17521/cjpe.2018.0063
[2] 王海珍,徐雅丽,代雅琦,韩路. 胡杨异形叶光合生理特性及其与叶形态的关系[J]. 塔里木大学学报,2020,32(3):35−43. doi: 10.3969/j.issn.1009-0568.2020.03.005 Wang HZ,Xu YL,Dai YQ,Han L. The photosynthetic physiology characteristics of heteromorphic leaves and their relationship with leaf shape in Populus euphratica[J]. Journal of Tarim University,2020,32(3):35−43. doi: 10.3969/j.issn.1009-0568.2020.03.005
[3] 张金玲. 臭柏对光胁迫的生理生态响应研究[D]. 保定:河北农业大学,2020:1−122. [4] Hao JQ,Yue N,Zheng CX. Analysis of changes in anatomical characteristics and physiologic features of heteromorphic leaves in a desert tree,Populus euphratica[J]. Acta Physiol Plant,2017,39(8):160. doi: 10.1007/s11738-017-2467-9
[5] 刘建丽. 常绿乔木圆柏的繁殖技术[J]. 新疆林业,2021(4):20−21. doi: 10.3969/j.issn.1005-3522.2021.04.008 [6] Tanaka-Oda A,Kenzo T,Kashimura S,Ninomiya I,Wang LH,et al. Physiological and morphological differences in the heterophylly of Sabina vulgaris Ant. in the semi-arid environment of Mu Us Desert,Inner Mongolia,China[J]. J Arid Environ,2010,74(1):43−48. doi: 10.1016/j.jaridenv.2009.07.013
[7] Zhang JL,Xu XH,Li XG,Li YL,Guy RD,Chen HP. Photoprotection in heteromorphic leaves of savin juniper (Juniperus sabina L.)[J]. Photosynthetica,2019,57(3):780−787. doi: 10.32615/ps.2019.097
[8] Zhang JL,Li XG,Xu XH,Chen HP,Li YL,Guy RD. Leaf morphology,photosynthesis and pigments change with age and light regime in savin juniper[J]. Plant Biol,2021,23(6):1097−1108. doi: 10.1111/plb.13256
[9] 王钰莹,魏梦瑶,焦梦晓,张奕蕾,邱念伟. 圆柏刺叶和鳞叶的光合功能比较[J]. 林业科技,2023,48(4):6−10,15. Wang YY,Wei MY,Jiao MX,Zhang YL,Qiu NW. Comparison of photosynthetic function between needle leaves and scale leaves of Sabina chinensis[J]. Forestry Science & Technology,2023,48(4):6−10,15.
[10] Renner SS,Ricklefs RE. Dioecy and its correlates in the flowering plants[J]. Am J Bot,1995,82(5):596−606. doi: 10.1002/j.1537-2197.1995.tb11504.x
[11] 贺俊东,胥晓,郇慧慧,杨帅,秦芳. 青杨雌雄扦插苗光合作用日变化与叶绿素荧光参数特征[J]. 植物研究,2014,34(2):219−225. He JD,Xu X,Huan HH,Yang S,Qin F. Characteristics of chlorophyll fluorescent parameters and daily dynamics of photosynthesis in female and male Populus cathayana cutting seedlings[J]. Bulletin of Botanical Research,2014,34(2):219−225.
[12] 唐学玺. 环境胁迫下雌雄异株植物的差异响应特征及研究进展[J]. 中国海洋大学学报,2020,50(7):74−81. Tang XX. Characteristics and research progress of sex-specific responses to environmental stresses of dioecious plants[J]. Periodical of Ocean University of China,2020,50(7):74−81.
[13] Zhang S,Chen LH,Duan BL,Korpelainen H,Li CY. Populus cathayana males exhibit more efficient protective mechanisms than females under drought stress[J]. For Ecol Manage,2012,275:68−78. doi: 10.1016/j.foreco.2012.03.014
[14] Xu X,Peng GQ,Wu CC,Korpelainen H,Li CY. Drought inhibits photosynthetic capacity more in females than in males of Populus cathayana[J]. Tree Physiol,2008,28(11):1751−1759. doi: 10.1093/treephys/28.11.1751
[15] Liu M,Liu XX,Kang JY,Korpelainen H,Li CY. Are males and females of Populus cathayana differentially sensitive to Cd stress?[J]. J Hazard Mater,2020,393:122411. doi: 10.1016/j.jhazmat.2020.122411
[16] Liao J,Cai ZY,Song HF,Zhang S. Poplar males and willow females exhibit superior adaptation to nocturnal warming than the opposite sex[J]. Sci Total Environ,2020,717:137179. doi: 10.1016/j.scitotenv.2020.137179
[17] Yang F,Wang Y,Wang J,Deng WQ,Liao L,Li M. Different eco-physiological responses between male and female Populus deltoides clones to waterlogging stress[J]. For Ecol Manage,2011,262(11):1963−1971. doi: 10.1016/j.foreco.2011.08.039
[18] Li CY,Ren J,Luo JX,Lu RS. Sex-specific physiological and growth responses to water stress in Hippophae rhamnoides L. populations[J]. Acta Physiol Plant,2004,26(2):123−129. doi: 10.1007/s11738-004-0001-3
[19] 孙晓伟. 温带3种雌雄异株树种光合特征对比[D]. 哈尔滨:东北林业大学,2022:1−62. [20] Marshall JD,Dawson TE,Ehleringer JR. Gender-related differences in gas exchange are not related to host quality in the xylem-tapping mistletoe,Phoradendron juniperinum (Viscaceae)[J]. Am J Bot,1993,80(6):641−645. doi: 10.1002/j.1537-2197.1993.tb15234.x
[21] Jones MH,MacDonald SE,Henry GHR. Sex-and habitat-specific responses of a high arctic willow,Salix arctica,to experimental climate change[J]. Oikos,1999,87(1):129−138. doi: 10.2307/3547004
[22] Dawson TE,Ward JK,Ehleringer JR. Temporal scaling of physiological responses from gas exchange to tree rings:a gender-specific study of Acer negundo (Boxelder) growing under different conditions[J]. Funct Ecol,2004,18(2):212−222. doi: 10.1111/j.0269-8463.2004.00838.x
[23] Letts MG,Phelan CA,Johnson DRE,Rood SB. Seasonal photosynthetic gas exchange and leaf reflectance characteristics of male and female cottonwoods in a riparian woodland[J]. Tree Physiol,2008,28(7):1037−1048. doi: 10.1093/treephys/28.7.1037
[24] Tozawa M,Ueno N,Seiwa K. Compensatory mechanisms for reproductive costs in the dioecious tree Salix integra[J]. Botany,2009,87(3):315−323. doi: 10.1139/B08-125
[25] 马文宝,廖成云,姬慧娟,陈雪,董廷发. 濒危连香树种群性比和雌雄株功能性状的差异[J]. 生态学杂志,2019,38(8):2414−2419. Ma WB,Liao CY,Ji HJ,Chen X,Dong TF. Sex ratio and sexual difference of functional traits in the endangered plant Cercidiphyllum japonicum[J]. Chinese Journal of Ecology,2019,38(8):2414−2419.
[26] 黄云浩,辛本花,王娟. 雌雄异株植物鼠李生殖分配与生殖耗费补偿机制[J]. 北京林业大学学报,2019,41(11):31−36. Huang YH,Xin BH,Wang J. Reproductive allocation and compensation mechanism for reproductive costs of dioecious shrub Rhamnus davurica[J]. Journal of Beijing Forestry University,2019,41(11):31−36.
[27] 陈银萍. 圆柏属植物抗冷冻适应性机制研究[D]. 兰州:兰州大学,2006:1−90. [28] 杨宗娟. 两种圆柏属植物叶片抗氧化系统对低温胁迫的响应机制研究[D]. 兰州:兰州交通大学,2013:1−69. [29] 路通. 圆柏叶挥发性有机物动态变化研究[D]. 晋中:山西农业大学,2022:1−58. [30] 宋晨慧,张有福,王梦可,王露露,陈春艳. 3种圆柏属植物叶片气孔特征对自然光强的响应[J]. 广东农业科学,2022,49(4):28−34. Song CH,Zhang YF,Wang MK,Wang LL,Chen CY. Response of leaf stomatal characteristics of three species of Juniperus to natural light intensity[J]. Guangdong Agricultural Sciences,2022,49(4):28−34.
[31] 韩兴华. 4种针叶树光合蒸腾特性的研究[D]. 呼和浩特:内蒙古农业大学,2007:1−39. [32] Ralph PJ,Gademann R. Rapid light curves:a powerful tool to assess photosynthetic activity[J]. Aquat Bot,2005,82(3):222−237. doi: 10.1016/j.aquabot.2005.02.006
[33] 冀宗琪. 蒙古栎非结构性碳水化合物在干旱胁迫中的调节作用[D]. 沈阳:沈阳农业大学,2022:1−60. [34] 段娜,贾玉奎,郝玉光,徐军,高君亮,陈海玲. 干旱胁迫对欧李叶绿素荧光特性的影响[J]. 西北林学院学报,2018,33(6):10−14. Duan N,Jia YK,Hao YG,Xu J,Gao JL,Chen HL. Effects of drought stress on chlorophyll fluorescence characteristics of Cerasus humilis[J]. Journal of Northwest Forestry University,2018,33(6):10−14.
[35] 朱成刚,陈亚宁,李卫红,付爱红,杨玉海. 干旱胁迫对胡杨PSⅡ光化学效率和激能耗散的影响[J]. 植物学报,2011,46(4):413−424. doi: 10.3724/SP.J.1259.2011.00413 Zhu CG,Chen YN,Li WH,Fu AH,Yang YH. Effect of drought stress on photochemical efficiency and dissipation of excited energy in photosystem Ⅱ of Populus euphratica[J]. Chinese Bulletin of Botany,2011,46(4):413−424. doi: 10.3724/SP.J.1259.2011.00413
[36] Liu LT,Li AC,Chen J,Wang M,Zhang YJ,et al. iTRAQ-based quantitative proteomic analysis of cotton (Gossypium hirsutum L.) leaves reveals pathways associated throughout the aging process[J]. Acta Physiol Plant,2019,41(8):144. doi: 10.1007/s11738-019-2921-y
[37] 董高峰,陈贻竹,李耿光,黄涛,阳成伟. 阳生植物和阴生植物的叶黄素循环与非辐射能量耗散[J]. 武汉植物学研究,2001,19(2):128−134. Dong GF,Chen YZ,Li GG,Huang T,Yang CW. Xanthophyll cycle and non-radiative energy dissipation in sun and shade plants[J]. Journal of Wuhan Botanical Research,2001,19(2):128−134.
[38] Lawson T,Blatt MR. Stomatal size,speed,and responsiveness impact on photosynthesis and water use efficiency[J]. Plant Physiol,2014,164(4):1556−1570. doi: 10.1104/pp.114.237107
[39] 张守仁. 叶绿素荧光动力学参数的意义及讨论[J]. 植物学通报,1999,16(4):444−448. Zhang SR. A discussion on chlorophyll fluorescence kinetics parameters and their significance[J]. Chinese Bulletin of Botany,1999,16(4):444−448.
[40] 王海珍,韩路,徐雅丽,刘艳萍,王琳. 胡杨异形叶光合系统Ⅱ叶绿素荧光特性[J]. 西北植物学报,2019,39(10):1795−1804. doi: 10.7606/j.issn.1000-4025.2019.10.1795 Wang HZ,Han L,Xu YL,Liu YP,Wang L. Chlorophyll fluorescence characteristics of photosystem Ⅱ of Populus euphratica heteromorphic leaves[J]. Acta Botanica Boreali-Occidentalia Sinica,2019,39(10):1795−1804. doi: 10.7606/j.issn.1000-4025.2019.10.1795
[41] 张瑞香. 不同林龄野生南方红豆杉碳氮磷生态化学计量与非结构性碳水化合物特征研究[D]. 郑州:河南农业大学,2023:1−52. [42] Quevedo-Rojas A,García-Núñez C,Jerez-Rico M,Jaimez R,Schwarzkopf T. Leaf acclimation strategies to contrasting light conditions in saplings of different shade tolerance in a tropical cloud forest[J]. Funct Plant Biol,2018,45(9):968−982. doi: 10.1071/FP17308
[43] 孙晓伟,王兴昌,孙慧珍,全先奎,杨青杰. 雌雄异株树种山杨、水曲柳和东北红豆杉光合特性对比[J]. 南京林业大学学报(自然科学版),2023,47(1):129−135. Sun XW,Wang XC,Sun HZ,Quan XK,Yang QJ. Photosynthetic characteristics of dioecious Populus davidiana,Fraxinus mandshurica and Taxus cuspidata[J]. Journal of Nanjing Forestry University (Natural Sciences Edition),2023,47(1):129−135.



 下载:
下载: