Comparison of the structure and photosynthetic characteristics of different photosynthetic organs in Trapa quadrispinosa Roxb.
-
摘要:
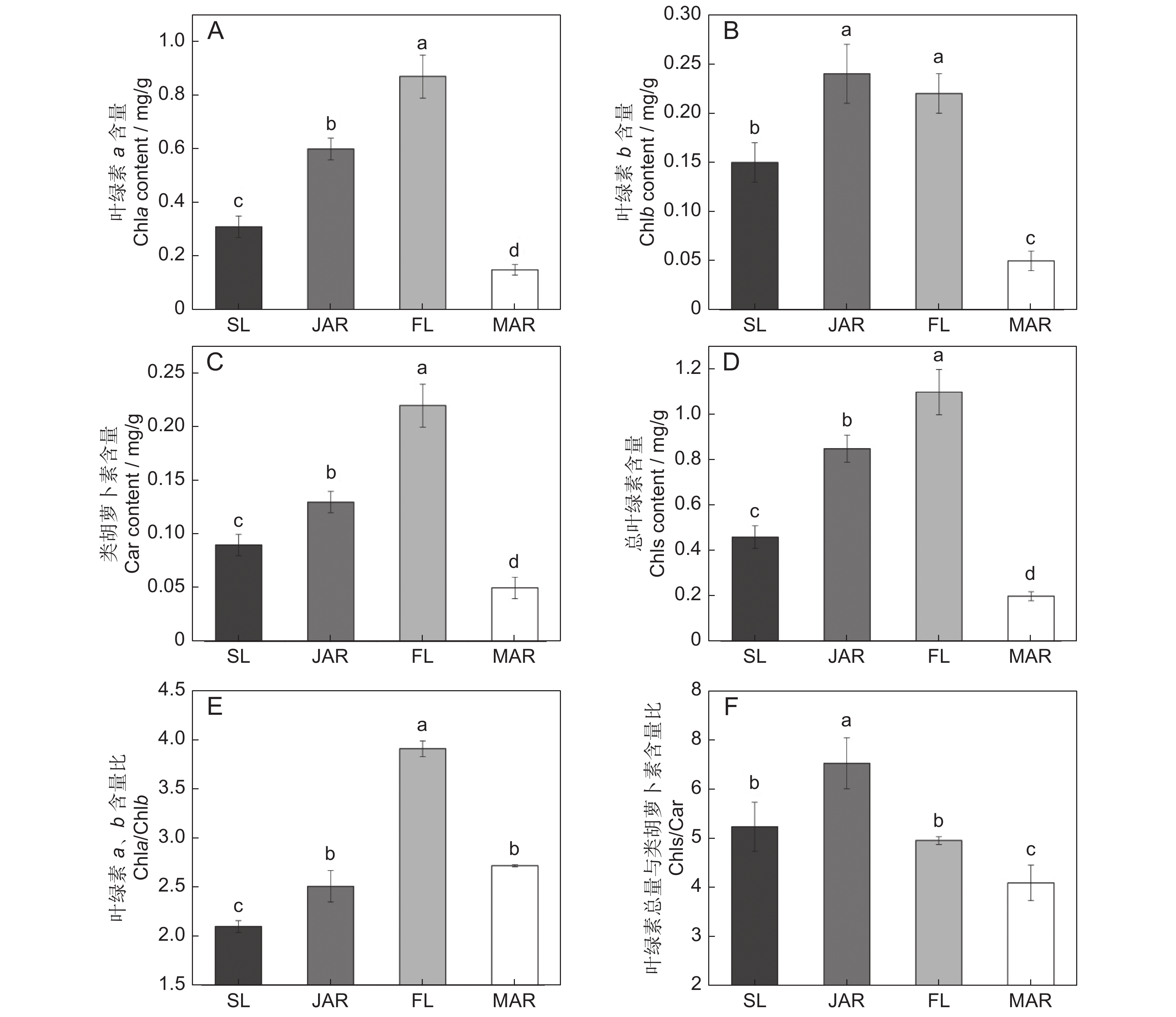
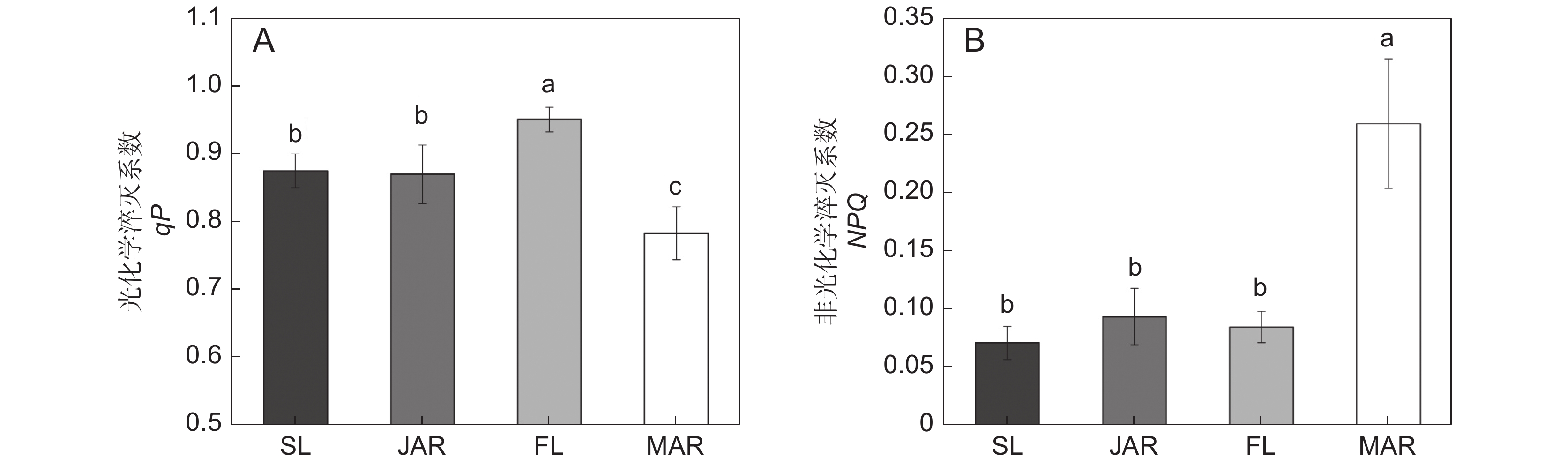
菱属(Trapa)植物具有沉水叶、浮水叶和不定根3种光合器官,且沉水叶仅出现于幼苗期。本文以常见野生菱属植物四角菱(T. quadrispinosa Roxb.)为实验材料,比较了不同光合器官在不同生长期的结构及光合特性差异。结果显示:(1)沉水叶结构简单,浮水叶为典型异面叶;(2)在幼苗期和成熟期,不定根均具有根的结构且含有叶绿体;3种光合器官的叶绿体大小及形态存在明显差异;(3)浮水叶的叶绿素a (Chla)、类胡萝卜素(Car)、总叶绿素(Chls)含量均显著高于其他组,幼苗期不定根和浮水叶的叶绿素b(Chlb)含量均显著高于其他组;(4)浮水叶的叶绿素荧光参数,包括最大光化学量子产量(Fv/Fm)、实际光化学量子产量(YⅡ)和光化学淬灭系数(qP),均显著高于其他组;(5)氧气交换速率分析结果显示,幼苗期不定根>沉水叶>浮水叶>成熟期不定根。综上所述,幼苗期四角菱的不定根光合能力高于沉水叶,成熟期的浮水叶光合能力高于不定根。
Abstract:The genus Trapa possesses three distinct photosynthetic organs, including submerged leaves, floating leaves, and adventitious roots. In this study, we compared the anatomical structures and photosynthetic characteristics of these organs at different growth stages of Trapa quadrispinosa Roxb. Results showed that: (1) Submerged leaves exhibited a simpler structure compared to the bifacial anatomy of floating leaves; (2) Adventitious roots at both the juvenile and mature stages retained typical root structures and evident chloroplasts; (3) Significant differences were observed in chloroplast size and morphology among submerged leaves, floating leaves, and adventitious roots; (4) Floating leaves contained significantly higher levels of chlorophyll a (Chla), carotenoid (Car), and total chlorophyll (Chls) compared to other organs, while juvenile adventitious roots and floating leaves exhibited higher chlorophyll b content (Chlb); (5) Floating leaves demonstrated superior photosynthetic efficiency, with higher maximum photochemical quantum yield (Fv/Fm), actual photochemical quantum yield (YⅡ), and photochemical quenching (qP) compared to the other organs. (6) Based on oxygen exchange rates, the order of the four photosynthetic organs from high to low was juvenile adventitious roots>submerged leaves>floating leaves>mature adventitious roots. Overall, during the seedling stage, photosynthetic capacity was higher in adventitious roots than in submerged leaves. In contrast, during the adult stage, floating leaves surpassed adventitious roots in photosynthetic capacity.
-
无居民海岛是指我国海域范围内不用于人口居住的岛屿[1],与有人居住的岛屿数量相比,我国有许多无人居住的岛屿,这些岛屿及周边海域拥有丰富的海洋资源,具有巨大的发展潜力,对我国海洋经济发展和资源合理利用具有重要作用[2]。岛屿植被是岛屿生态系统的重要组成部分,了解岛屿的植物资源对于确定植被的恢复和建设方式具有指导意义[3]。近年来,国内对无居民海岛植被的研究日益增多,主要集中于无居民海岛植物群落的相关环境因子[4-6]、外来入侵植物[7]和海岛开发利用[8-10]等方面。然而,目前对无居民海岛植物物种组成及区系特征的相关研究报道较少。
本研究在实地调查和查阅以往文献的基础上,总结分析了福建平潭5个无居民海岛的种子植物物种组成和地理分布型类型,探索该地区种子植物区系的组成和地理分布,研究结果旨在为保护海岛特色植物群落、促进海岛生态规划和创造海岛优质生态环境提供线索。
1. 材料与方法
1.1 研究区概况
平潭为福建省管辖的综合实验区,位于福建省东部,是福建省第一大岛。平潭属亚热带季风气候,夏季主要为西南风,冬季以东北风为主[11]。本次调查选取包括光幼屿(25°34′54.48″N,119°50′4.56″E)、红山屿(25°34′41.88″N,119°50′27.96″E)、黄门岛(25°27′40.68″N,119°40′ 50.88″E)、姜山岛(25º26′30.12″N,119º48′28.30″E)、龙母屿(25°20′49.26″N,119º41′48.74″E)在内的5座无居民海岛,各岛概况见表1。
表 1 平潭5个无居民海岛基本情况Table 1. Basic information of 5 uninhabited islands in Pingtan岛屿
Island面积
Area / hm²近岸距离
Inshore distance / km周长
Perimeter / m海拔
Altitude / m周长/面积
Perimeter area ratio物种数
Species光幼屿 6.22 22.57 1 075.4 45.1 0.017 77 红山屿 3.07 23.05 1 015.0 33.2 0.033 53 黄门岛 7.18 3.89 1 417.3 24.2 0.020 114 姜山岛 40.24 1.12 4 951.2 22.4 0.012 115 龙母屿 2.88 8.14 993.3 20.8 0.034 102 1.2 调查对象及方法
本研究采用样方法和样线法相结合的技术路线,对平潭5个无居民海岛的植物资源进行详尽的全面踏勘。样方法设置的乔木群落样方面积为20 m×20 m,共22个,四角设置4个5 m×5 m的灌木样方,另外取5个1 m×1 m的草本样方,分别位于样地的四角及中部位置。样线法设置方法为按环岛样线和东西向或南北向沿岛屿中部设置样线的方式,记录样线左右10 m以内出现的植物。随时记录沿路所见植物种类,拍摄照片,对于现场无法识别的植物记录其细节特征,查阅《福建植物志》[12]进行鉴定。依据中国外来入侵物种信息系统(http://www.iplant.cn/ias)和《中国入侵植物名录》[13] 统计外来植物。采用《世界种子植物科的分布区类型》[14]划分种子植物科分布区类型,属、种的分布区类型根据《中国种子植物属的分布区类型》[15] 并结合中国植物志电子版(https://www.iplant.cn/)进行划分。
剔除外来植物后,根据以上方法划分该地种子植物科属种的分布区类型,分析其种子植物区系特征。通过热带属数/温带属数(R/T)研究其区系成分,以平潭5个无居民海岛与其他无居民海岛属的分布区类型为基础,进行聚类分析。采用Jaccard 相似性系数[16],分别计算平潭5个无居民海岛之间的属-种相似性系数,并对岛屿空间特征参数的相关性进行分析。以上数据处理均利用Excel 2016和SPSS 26软件完成。
2. 结果与分析
2.1 平潭5个无居民海岛的种子植物物种组成
调查发现,5个无居民海岛共有种子植物213种(含种下单位,下同),隶属71科179属。其中,被子植物70科178属212种;裸子植物仅1种;单子叶植物10科33属48种,分别占总科、属、种数的14.08%、18.44%和22.54%;双子叶植物61科146属165种,分别占总科、属、种数的85.92%、81.56%和77.46%(表2)。
表 2 平潭5个无居民海岛种子植物物种分类群统计Table 2. Statistics of vascular plant species taxa of 5 uninhabited islands in Pingtan分类群
Plant taxon科数(占比)
No. of families(Percentage / %)属数(占比)
No. of genera(Percentage / %)种数(占比)
No. of species(Percentage / %)裸子植物 1(1.41) 1(0.56) 1(0.47) 被子植物 70(98.59) 178(99.44) 212(99.53) 双子叶植物 61(85.92) 146(81.56) 165(77.46) 单子叶植物 10(14.08) 33(18.44) 48(22.54) 合计 71(100) 179(100) 213(100) 根据整理的种子植物名录,外来草本植物共有42种(19.72%),隶属于20科38属,如鬼针草(Bidens Pilosa L.)、飞扬草(Euphorbia hirta L.)、蟛蜞菊(Wedelia chinensis (L.) Pruski)、牵牛(Pharbitis ni (L.) Roth)和白花地胆草(Elephantopus tomentosus L.)等;原生草本植物共有171种(80.28%),隶属于65科145属。可见,平潭5个无居民海岛的种子植物以原生植物分布为主。
2.2 种子植物生活型统计与分析
植物生活型是植物对环境长期适应的表现形式,体现在外部形态、结构等方面,可反映植物与环境间的关系[17, 18],并揭示植物对环境的生态适应性[19]。由表3可知,植物生活型有乔木、灌木、藤本和草本4种类型。平潭5个无居民海岛的种子植物生活型占比大小依次是草本(59.65%)、灌木(28.07%)、藤本(8.19%)和乔木(4.09%)。草本植物种数最多,其中,多年生草本58种,包括烟豆(Glycine tabacina Benth)、中华补血草(Limonium sinense (Girard) Kuntze)和厚藤(Ipomoea pes-caprae (L.) R. Brown)等;一、二年生植物44种,分别占总种数的21.64%和4.09%,包括画眉草(Eragrostis pilosa (L.) Beauv)、马唐(Digitaria sanguinalis (L.) Scop)和爵床(Justicia procumbens L.)等。
表 3 平潭5个无居民海岛种子植物种子植物生活型统计Table 3. Statistics of life forms of seed plants of 5 uninhabited islands in Pingtan生活型
Life form种数
No. of species占总种数的百分比
Account of total species / %乔木 常绿 2 1.17 落叶 5 2.92 灌木 常绿 31 18.13 落叶 17 9.94 藤本 常绿木质藤本 5 2.92 落叶木质藤本 4 2.34 多年生草质藤本 5 2.92 草本 一年生 37 21.64 二年生 7 4.09 多年生 58 33.92 合计 171 100 2.3 种子植物区系地理成分统计与分析
2.3.1 科分布区类型
在科水平上,平潭5个无居民海岛种子植物65科的地理成分可划分为6个类型4个变型(表4)。其中,世界广布科有29个,占总科数的44.62%,包括菊科、禾本科、蔷薇科、苋科和蝶形花科等。科的地理分布中热带成分占比优势显著,热带性质突出。经统计,热带性质科共28个,占总科数(除世界广布科)的77.78%。热带性质的科主要有大戟科、夹竹桃科、锦葵科和含羞草科等。温带性质的科共8个,包括忍冬科和胡颓子科等,占总科数(除世界广布科)的22.22%。
表 4 平潭5个无居民海岛科、属、种的分布区类型统计Table 4. Distribution pattern statistics of vascular plants families, genera and species on five uninhabited islands in Pingtan分布区类型及其变型
Distribution types and variants科
Families属
Genera种
Species数量
No.占比
Percentage / %数量
No.占比
Percentage / %数量
No.占比
Percentage / %1. 世界分布 29 – 15 – 7 – 2. 泛热带分布 23 63.89 52 40.00 16 9.76 2-1. 热带亚洲-大洋洲和热带美洲分布 1 2.78 2 1.54 1 0.61 2-2. 热带亚洲、非洲和南美洲间断分布 1 2.78 4 3.08 5 3.05 2S. 以南半球为主的泛热带 1 2.78 0 0 0 0 3. 热带亚洲和热带美洲间断分布 1 2.78 4 3.08 7 4.27 4. 旧世界热带分布 1 2.78 14 10.77 6 3.66 4-1. 热带亚洲、非洲和大洋洲间断或星散分布 0 0 2 1.54 3 1.83 5. 热带亚洲至热带大洋洲分布 0 0 8 6.15 19 11.59 6. 热带亚洲至热带非洲 0 0 2 1.54 4 2.44 7. 热带亚洲(印度-马来西亚)分布 0 0 2 1.54 29 17.68 8. 北温带分布 4 11.11 14 10.78 7 4.27 8-4. 北温带和南温带(全温带)间断分布 3 8.33 3 2.31 3 1.83 9. 东亚和北美洲间断分布 0 0 6 4.62 4 2.44 10. 旧世界温带分布 0 0 4 3.08 4 2.44 10-1. 地中海区、西亚(或中亚)和东亚间断分布 0 0 3 2.31 1 0.61 10-3. 欧亚和南部非洲(有时也在大洋洲)间断分布 0 0 1 0.77 0 0 11. 温带亚洲 0 0 0 0 17 10.37 14. 东亚分布 1 2.78 7 5.38 14 8.54 14-1. 中国-喜马拉雅(SH) 0 0 0 0 3 1.83 14-2. 中国-日本(SJ) 0 0 1 0.77 9 5.49 15. 中国特有分布特有 0 0 1 0.77 12 7.32 合计 65 100 145 100 171 100 2.3.2 属分布区类型
在属水平上,平潭5个无居民海岛的种子植物共145属,其地理成分可划分为12个类型7个变型(表4)。世界广布类型的属有15个,占总属数的10.34%,包括莎草属(Cyperus)、苋属(Amaranthus)和马唐属(Digitaria)等。属的分布区类型中热带成分占主导地位,有90个,占总属数(除世界广布属)的69.24%,热带性质明显,包括大戟属(Euphorbia)、南蛇藤属(Celastrus)、紫珠属(Callicarpa)和马齿苋属(Portulaca)等。温带性质的属共40个,占总属数(除世界广布属)的30.02%,包括山麦冬属(Liriope)、胡枝子属(Lespedeza)、胡颓子属(Elaeagnus)和络石属(Trachelospermum)等。
2.3.3 种分布区类型
在种水平上,平潭5个无居民海岛共有171种种子植物(不含外来植物),其地理成分可划分为13个分布区类型7个变型(表4)。世界广布类型的种有7个,占总种数的4.09%,如莎草属(Cyperus)、苋属(Amaranthus)和堇菜属(Viola)等。种的分布区类型中热带成分占主导地位,热带性质(2~7型)的种有90个,占总种数(除世界广布种)的54.88%,热带性质明显,包括马蹄金(Dichondra micrantha Urban)、紫珠(Callicarpa bodinieri Levl)和算盘子(Glochidion puberum (L.) Hutch)等。温带性质(8~14型)的种共62个,占总种数(除世界广布种)的37.80%,有桑(Morus alba L.)、滨柃(Eurya emarginata (Thunb.) Makino)和络石(Trachelospermum jasminoides (Lindl.) Lem)等。
2.3.4 滨海特有植物
仅分布于岛屿或滨海地区且具有明显岛屿特征的植物被称为滨海特色植物[20]。由于海岛的特殊环境结构,平潭5个无居民海岛分布有较多的滨海特色植物,共14科24属24种。其中,滨海前胡(Peucedanum japonicum Thunb)、滨柃(Eurya emarginata (Thunb.) Makino)、肉叶耳草(Hedyotis coreana (DC.) Neupane & N. Wikstr)和滨海珍珠菜(Lysimachia mauritiana Lam)等植物既适应海岛的气候与土壤,又具有滨海特色与观赏价值,同时具有较高的园林利用价值和极高的生态价值。
2.4 平潭5个无居民海岛与其他海岛种子植物区系比较分析
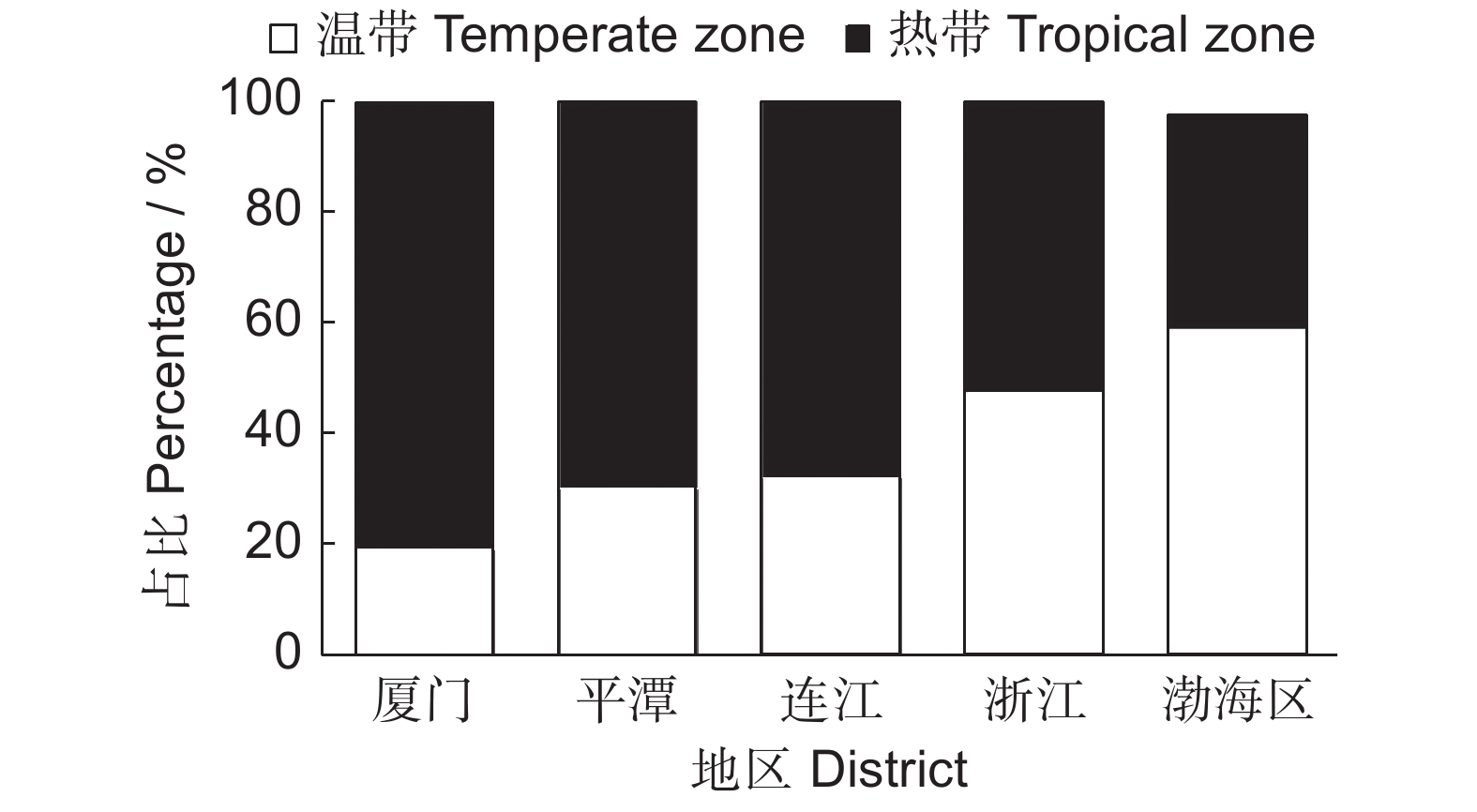
对平潭5个无居民海岛与其他海岛区系进行种子植物属的分布区类型比较,结果见表5。各个地区中泛热带分布型占比较高,为24.03%~40.00%,厦门近岸海域无居民海岛植物区系的R/T值(4.23)远高于其他海岛,热带性质最强烈;纬度相近的平潭和连江无居民海岛的R/T值接近,且均大于2,分别为2.31和2.13,热带优势明显。相反,纬度相对较高的浙江无居民海岛和渤海区9个无居民海岛的热带成分比例稍低,而温带分布比例略高,R/T值最低,仅为1.11和0.66,两者的北温带分布比例则远高于前三者,温带性质趋势明显,符合R/T值的排列顺序。将世界分布属和中国特有属排除后,重新计算这些地区的R/T值(图1)。由图1可知,随着纬度的增加,热带分布型所占比例逐渐降低,而温带分布型占比则逐渐上升,植物区系具有热带向温带过渡的特点,与中国植被类型的分布规律一致[21]。
表 5 平潭与其他地区无居民海岛种子植物属的分布区类型比较Table 5. Comparison of distribution types of seed flora and genera among five uninhabited islands in Pingtan and different island regions分布区
类型
Distribution type平潭(5个)
Pingtan (5)
(25°15′~25°45′N)厦门近岸
Xiamen
(24°25′~24°35′N)连江(5个)
Lianjiang (5)
(26°07′~26°27′N)浙江(5个)
Zhejiang (5)
(28°12′~28°18′N)渤海(9个)
Bohai Sea
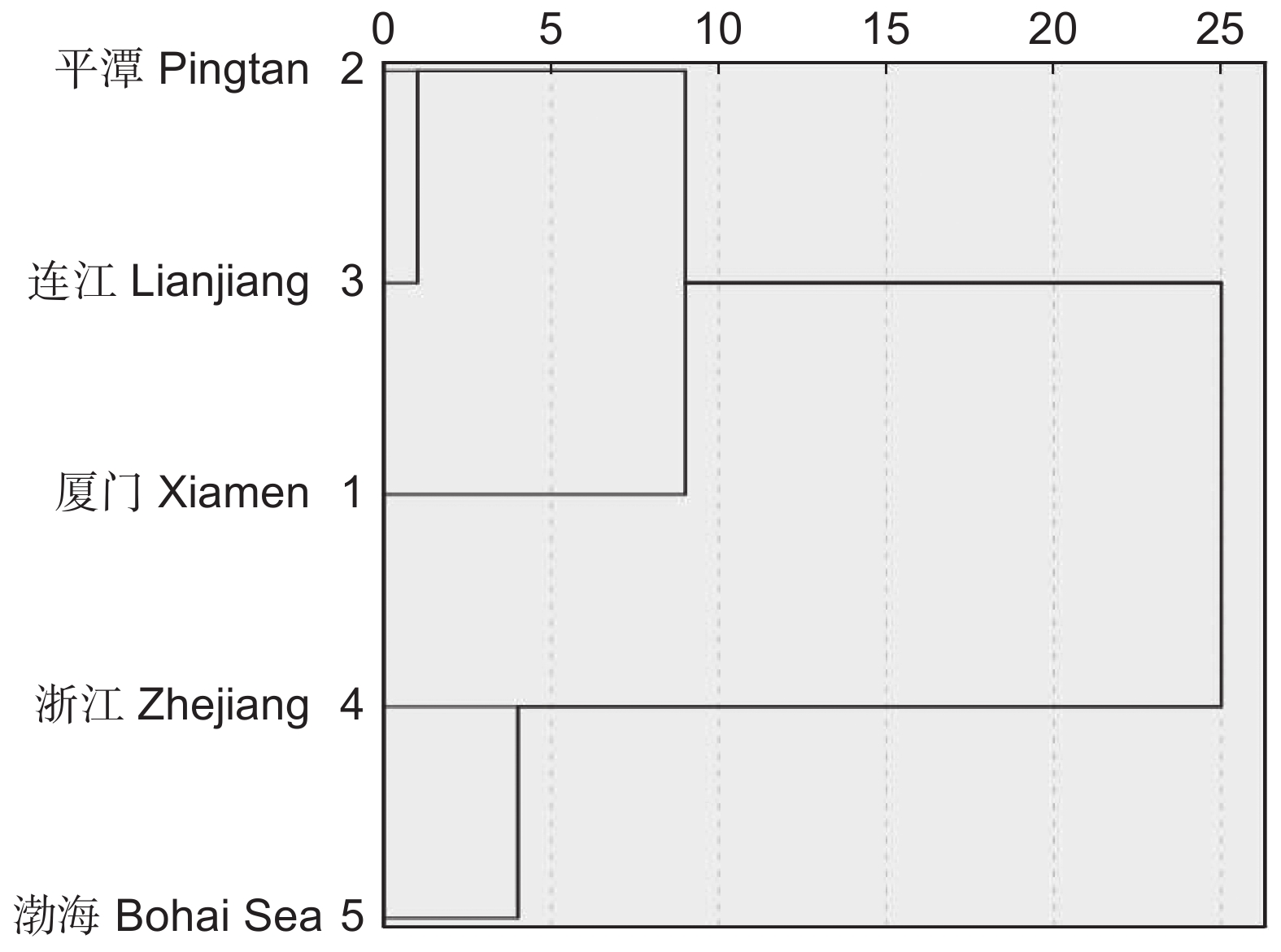
(37°06′~40°55′N)1 10.34 9.35 10.90 12.34 16.67 2 40.00 29.50 36.05 24.03 24.71 3 2.76 11.87 7.48 1.30 0.00 4 11.03 8.63 8.16 7.14 4.71 5 5.52 8.99 6.80 5.19 2.35 6 1.38 6.83 4.08 5.19 3.53 7 1.38 7.19 5.44 3.25 3.53 8 11.72 7.91 13.60 23.38 30.59 9 4.14 3.24 4.08 4.55 5.88 10 5.52 2.16 5.44 4.55 9.41 11 0.00 0.00 0.68 0.64 5.88 12 0.00 0.36 0.00 0.00 2.35 13 0.00 0.00 0.00 0.00 0.00 14 5.52 3.60 8.16 8.44 4.71 15 0.69 0.36 0.00 0.00 2.35 R/T 2.31 4.23 2.13 1.11 0.66 注:1,世界广布;2,泛热带分布;3,热带亚洲和热带美洲分布;4,旧世界热带分布;5,热带亚洲至热带大洋洲分布;6,热带亚洲至热带非洲分布;7,热带亚洲分布;8,北温带分布;9,东亚和北美间断分布;10,旧世界温带分布;11,温带亚洲分布;12,地中海及西亚至中亚分布;13,中亚分布;14,东亚分布;15,中国特有分布。 Notes: 1, Cosmopolitan; 2, Pantropic; 3, Tropical Asia & tropical America disjunct; 4, Old world tropical distributed; 5, Tropical Asia to tropical Australasia distributed; 6, Tropical Asia to tropical Africa distributed; 7, Tropical Asia distributed; 8, North temperate distributed; 9, East Asia & North America disjunct; 10, Old world temperate distributed; 11, Temperate Asia; 12, Mediterranea, West Asia to Central Asia; 13, Central Asia; 14, East Asia distributed; 15, Endemic to China. 为进一步探讨平潭5个无居民海岛与其他地区植物区系的相似性,对其属的分布区类型比率进行聚类分析。如图2所示,当欧氏距离约为10时,可将5个地区划分为2组。第1组为厦门近岸海域无居民海岛、平潭5个无居民海岛和连江县5个无居民海岛,3个地区纬度相近,植物热带成分占50%以上;第2组为渤海区9个无居民海岛和浙江5个无居民海岛,其植物热带成分明显减少,占30%左右。
2.5 不同岛屿间植物的物种相似度与空间特征关系
计算平潭5个无居民海岛属相似性系数与种相似性系数。结果显示,5个海岛在属级水平上相似性程度均不高,属的相似性系数大于30%的有光幼屿分别与红山屿(48%)和黄门岛(32%);以及姜山岛分别与龙母屿(47%)和黄门岛(31%);相似性系数小于30%的有黄门岛与红山屿(28%)、姜山岛分别与光幼屿(21%)和红山屿(20%),龙母屿分别与光幼屿(26%)、红山屿(22%)、黄门岛(28%)(附表1
1 ))。相较于属级水平,各个海岛之间在种级水平上的相似性程度有所降低,姜山岛与光幼屿(19%)以及红山屿(17%)之间的相似度均小于20%,说明这3个海岛在种水平上的差异较大(附表
1 ))。分析物种相似性系数Cj与岛屿空间特征的相关性,结果表明,Cj与面积比(δA)(0.577)、岸线长度比(δPer)(0.585)和高程比(δE)(0.591)呈正相关,与周长面积比的比值(δPAR)(−0.602)和近岸距离比(δI)(−0.211)呈负相关,但均不显著。
3. 讨论
3.1 平潭5个无居民海岛种子植物区系特征
平潭5个无居民海岛的种子植物共有71科179属213种,剔除外来物种后,共65科145属171种,与福建种子植物202科1596属4416种相比[22],本研究区域种子植物的科、属 、种数分别占了福建省植物区系的32.18%、9.09%和3.87%。按照生活型进行分类,草本植物占优势,共计102种(59.65%);其次为灌木48种(28.07%);乔木和藤本的种数则较少,分别是7种(4.09%)和14种(8.19%)。
平潭海岛的种子植物区系优势较为明显,含有较多热带科以及亚热带科,区系科、属、种的地理性质均以热带为主,科的热带成分占77.79%,温带成分仅占22.22%;属的热带成分占69.24%,温带成分为30.02%;种的热带成分占54.88%,温带成分为37.80%。种子植物中含有较多的热带科以及亚热带科,与福建省植物区系的特征相符合。科、属的热带成分以泛热带分布为主,种的热带成分以热带亚洲为主;科、属的温带成分以北温带为主,种的温带成分以温带亚洲及东亚分布为主,整体呈现显著的由热带向温带过渡的趋势。通过对平潭与其他地区岛屿的属分布区类型进行对比发现,除浙江和渤海区的无居民海岛外,其余岛屿的R/T值均具有明显的热带性质,符合其所处的亚热带海洋季风气候区的地理位置及热带起源[23],这一结果与相关研究[24]一致。随着纬度的增加,不同海岛植物区系的属级分布类型中,温带分布型逐渐增加,热带分布型占比逐步减少,显示出海岛植物区系地理成分的纬向分异性。
3.2 平潭5个无居民海岛间植物的物种相似度与空间特征关系
分析平潭5个无居民海岛植物间的种相似性系数及其与岛屿空间特征的相关性,发现Cj与面积比、岸线长度比和高程等空间特征均无显著相关性。平潭5个无居民海岛中,物种组成相似性较高的有光幼屿与红山屿、姜山岛与龙母屿、黄门岛与光幼屿,以及姜山岛与黄门岛,但均未超过50%,说明各个岛屿植物间的亲缘关系较远。
通常海岛面积越大,环境异质性越高,物种丰富度也会更高,这是岛屿生物地理学的普遍规律[25, 26]。平潭5个无居民海岛中姜山岛的面积最大,物种数也最多。但面积最小的龙母屿,其物种数却居第3,原因之一可能是龙母屿的灌木、草本能够较好地适应岛屿环境,且草本植物在该岛占绝对优势[27],其生存所需空间比乔木小得多,所以受岛屿面积的制约较小[28, 29];另一方面,尽管平潭5个无居民海岛同属一个气候带,但不同海岛间的物种数存在差异主要是由海岛环境的特殊性决定的[30]。
由于各个岛屿具有独立性,形成了不同的生态环境,并进行长时间的自然选择[31, 32],因此导致各岛屿的植物种类存在差异。本文仅以分布型从宏观层面对平潭5个无居民海岛的种子植物进行了区系分析,没有从微观层面进行探讨,后期对植物区系的研究可考虑土壤因子、地质变化和岛屿间植物竞争生态位等方面的因素。
3.3 平潭5个无居民海岛的保护和利用
海岛植物物种丰富度与人为活动因素紧密相关[33]。有居民海岛由于长期受人为干扰,海岛植被中的原生植被可能被破坏,从而对原生植物的生态位造成威胁,此外,海岛开发也会导致一定程度上原生植物数量的减少和次生植被的增加[34]。相比有居民海岛,无居民海岛植物受人为干扰较小。
平潭5个无居民岛屿的种子植物以原生植物为主,但海岛上的入侵植物也需要重视,如鬼针草(Bidens pilosa L.)、马缨丹(Lantana camara L.)和小蓬草(Conyza canadensis L.)等。为保护当地的物种多样性,避免物种的进一步同质化[35],应建立一个长期稳定的实时更新数据库,开展生态治理研究[36]。针对以上入侵植物,建议制定具有针对性的防控策略,尽可能挖掘其潜在的利用价值[37],做到有效防控与利用。
1 如需查阅附图内容请登录《植物科学学报》网站(http://www.plantscience.cn)查看本期文章。2 1~2)如需查阅附图内容请登录《植物科学学报》网站(http://www.plantscience.cn)查看本期文章。3 如需查阅附图内容请登录《植物科学学报》网站(http://www.plantscience.cn)查看本期文章。4 )如需查阅附图内容请登录《植物科学学报》网站(http://www.plantscience.cn)查看本期文章。 -
图 1 不同器官光合色素含量
SL:沉水叶;JAR:幼苗期不定根;FL:浮水叶;MAR成熟期不定根。不同小写字母表示不同器官在P<0.05水平上差异显著。下同。
Figure 1. Photosynthetic pigment content in different types of organs
SL: Submerged leaves; JAR: Juvenile adventitious roots; FL: Floating leaves; MAR: Mature adventitious roots. Different lowercase letters indicate significant differences at P<0.05 level among different organs. Same below.
表 1 不同类型叶片的横切结构特征
Table 1 Transverse structure characteristics of submerged and floating leaves of Trapa quadrispinosa
类型
Type叶片厚度
Leaf thickness / μm上表皮厚度
Upper epidermal thickness / μm上表皮细胞面积
Upper epidermal cell area / μm2下表皮厚度
Lower epidermal thickness / μm下表皮细胞面积
Lower epidermal cell area / μm2沉水叶 259.582±44.738a 6.824±1.674a 51.913±20.686a 7.000±2.081a 52.859±19.435a 浮水叶 192.644±3.921b 8.296±0.975b 65.408±15.473b 6.075±1.049b 42.722±15.551b 注:同列不同小写字母表示在P<0.05水平上差异显著。下同。 Note: Different lowercase letters in the same column indicate significant differences at P<0.05 level. Same below. 表 2 不同阶段不定根的横切结构特征
Table 2 Transverse structure characteristics of adventitious roots at different stages
类型
Type截面面积
Section area / μm2截面直径
Section diameter / μm外表皮厚度
Exodermis thickness / μm外表皮细胞面积
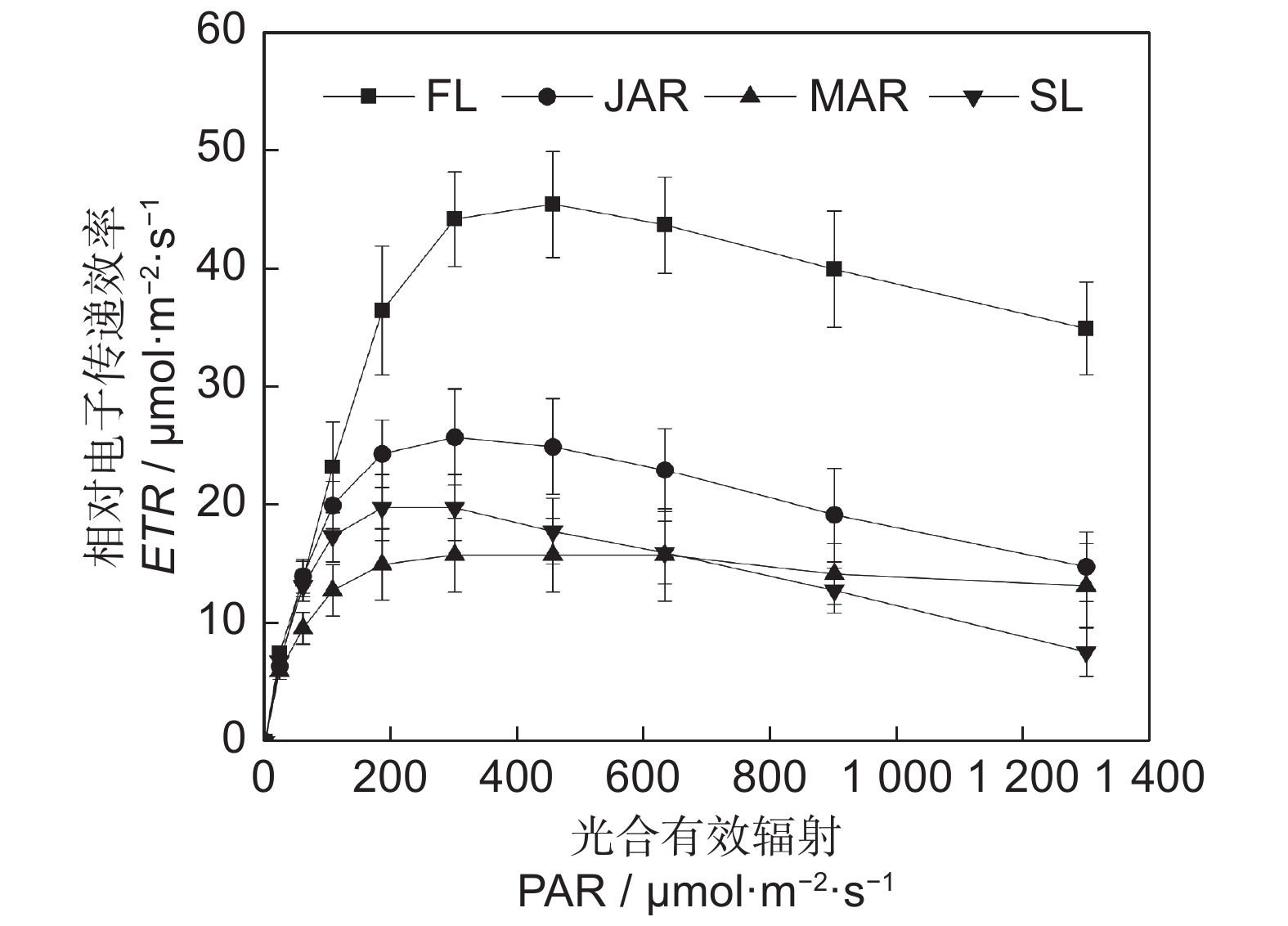
Exodermis cell area / μm2幼苗期不定根 59 216.650±128.654a 273.789±5.008a 3.836±0.768a 20.025±5.620a 成熟期不定根 29 316.670±187.506b 192.325±10.232b 1.530±0.610b 7.405±3.050b 表 3 不同光合器官的快速光曲线参数
Table 3 RLC parameters of different types of organs
器官类型
Organ types初始斜率
α最大相对电子
传递效率
ETRmax半饱和光强
IK沉水叶 0.300±0.035a 20.420±2.961bc 68.160±7.973bc 苗期不定根 0.312±0.019a 26.300±3.780b 84.160±9.766b 浮水叶 0.285±0.048a 43.700±7.119a 156.680±33.315a 成熟期不定根 0.316±0.028a 16.960±3.204c 53.600±7.997c -
[1] Li GJ,Hu SQ,Hou HW,Kimura S. Heterophylly:phenotypic plasticity of leaf shape in aquatic and amphibious plants[J]. Plants,2019,8(10):420. doi: 10.3390/plants8100420
[2] Wang SN,Li PP,Liao ZY,Wang WW,Chen T,et al. Adaptation of inorganic carbon utilization strategies in submerged and floating leaves of heteroblastic plant Ottelia cordata[J]. Environ Exp Bot,2022,196:104818. doi: 10.1016/j.envexpbot.2022.104818
[3] 金泉,李鹏鹏,张瑞花,尹黎燕. 水菜花异形叶片叶绿素荧光特征与HCO3-利用能力的研究[J]. 植物科学学报,2019,37(5):637−643. Jin Q,Li PP,Zhang RH,Yin LY. Chlorophyll fluorescence characteristics and HCO3- utilization capability of heteromorphic leaves of Ottelia cordata[J]. Plant Science Journal,2019,37(5):637−643.
[4] 卫沙沙,李鹏鹏,袁龙义,李伟,江红生. 叶异形水生植物不同发育阶段叶片的结构和无机碳获取策略[J]. 植物科学学报,2022,40(4):544−552. Wei SS,Li PP,Yuan LY,Li W,Jiang HS. Leaf structure and inorganic carbon acquisition strategies of heteroblastic aquatic plants at different stages of development[J]. Plant Science Journal,2022,40(4):544−552.
[5] 万文豪. 中国菱科植物分类研究[J]. 南昌大学学报(理科版),1984,8(2):71−78. [6] 丁炳杨,李平,方云亿. 菱属植物沉水叶和不定根的观察[J]. 植物学报,1988(3):140−142. [7] 陆昌燕,刘体育,郑兴峰. 四角菱根系的发育和功能[J]. 安徽农业科学,2011,39(8):4416−4417. Lu CY,Liu TY,Zheng XF. Development and function of root system of Trapa quadrispinosa Roxb.[J]. Journal of Anhui Agricultural Sciences,2011,39(8):4416−4417.
[8] 曾宪锋,周仪. 关于菱的沉水茎上不定根的探讨[J]. 生物学通报,1996(9):28. [9] Nedukha OM. Anatomical structure of Trapa natans L. submerged organs in context of the species ecology[J]. Mod Phytomorphol,2015,8:153−160.
[10] Arima S,Tanaka N,Kubota F. Growth and photosynthetic rate of water roots of water chestnut (Trapa bispinosa Roxb.)[J]. Bull Fac Agric,Saga Univ,1988(64):27−35.
[11] 王婉婉,陆镇威,袁龙义,江红生. 纳米银对紫萍休眠芽萌发、存活和生长的影响[J]. 植物科学学报,2022,40(4):576−583. Wang WW,Lu ZW,Yuan LY,Jiang HS. Effects of silver nanoparticles on dormant bud germination,seedling survival,and growth of Spirodela polyrhiza (L.) Schleid[J]. Plant Science Journal,2022,40(4):576−583.
[12] 王婉婉. 纳米银对水生植物紫萍光合作用毒性效应及作用机制[D]. 荆州:长江大学,2022:15. [13] Li PP,Liao ZY,Zhou JZ,Yin LY,Jiang HS,Li W. Bicarbonate-use by aquatic macrophytes allows a reduction in photorespiration at low CO2 concentrations[J]. Environ Exp Bot,2021,188:104520. doi: 10.1016/j.envexpbot.2021.104520
[14] 王德华. 水生植物的定义与适应[J]. 生物学通报,1994,29(6):10. [15] 王晨,李龙,倪细炉,李健. 穿叶眼子菜茎叶结构及其通气组织发育解剖学研究[J]. 西北植物学报,2018,38(7):1279−1287. Wang C,Li L,Ni XL,Li J. Study on the developmental anatomy of structures and aerenchyma formation in Potamogeton perfoliatus stems and leaves[J]. Acta Botanica Boreali-Occidentalia Sinica,2018,38(7):1279−1287.
[16] 罗玉明,丁小余,杨晋彬,施国新. 菱的腺毛发育及分泌活动的超微结构研究[J]. 广西植物,2006,26(4):352−355. Luo YM,Ding XY,Yang JB,Shi GX. Studies on the development of glandular hairs in Trapa bispinosa and the ultrastructure during their secretory activity[J]. Guihaia,2006,26(4):352−355.
[17] 杨宽. 6种睡莲叶片解剖结构及耐寒性评价[J]. 分子植物育种,2021,19(20):6910−6917. Yang K. Leaf anatomic structure and cold tolerance evaluation of 6 Nymphaea varieties[J]. Molecular Plant Breeding,2021,19(20):6910−6917.
[18] Kordyum E,Mosyakin S,Ivanenko G,Ovcharenko Y,Brykov V. Hydropotes of young and mature leaves in Nuphar lutea and Nymphaea alba (Nymphaeaceae):formation,functions and phylogeny[J]. Aquat Bot,2021,169:103342. doi: 10.1016/j.aquabot.2020.103342
[19] 汪攀,陈奶莲,邹显花,马祥庆,吴鹏飞. 植物根系解剖结构对逆境胁迫响应的研究进展[J]. 生态学杂志,2015,34(2):550−556. Wang P,Chen NL,Zou XH,Ma XQ,Wu PF. Research progress on adaptive responses of anatomical structure of plant roots to stress[J]. Chinese Journal of Ecology,2015,34(2):550−556.
[20] Rich SM,Ludwig M,Colmer TD. Photosynthesis in aquatic adventitious roots of the halophytic stem-succulent Tecticornia pergranulata (formerly Halosarcia pergranulata)[J]. Plant Cell Environ,2008,31(7):1007−1016. doi: 10.1111/j.1365-3040.2008.01813.x
[21] 高佳,崔海岩,史建国,董树亭,刘鹏,等. 花粒期光照对夏玉米光合特性和叶绿体超微结构的影响[J]. 应用生态学报,2018,29(3):883−890. Gao J,Cui HY,Shi JG,Dong ST,Liu P,et al. Effects of light intensities after anthesis on the photosynthetic characteristics and chloroplast ultrastructure in mesophyll cell of summer maize (Zea mays L.)[J]. Chinese Journal of Applied Ecology,2018,29(3):883−890.
[22] 李晨,刘建廷,樊永信,赵雪惠,肖伟,等. UV-B对设施桃叶片光合功能及叶绿体超微结构的影响[J]. 植物学报,2022,57(4):434−443. Li C,Liu JT,Fan YX,Zhao XH,Xiao W,et al. Effects of UV-B on photosynthetic function and chloroplast ultrastructure of peach leaves grown in greenhouse[J]. Chinese Bulletin of Botany,2022,57(4):434−443.
[23] 袁秀云,许申平,周一冉,王喜蒙,崔波. 遮荫对白及形态及叶片结构的影响[J]. 植物研究,2021,41(6):974−981. Yuan XY,Xu SP,Zhou YR,Wang XM,Cui B. Shading effect on morphology and leaf structure of Bletilla striata[J]. Bulletin of Botanical Research,2021,41(6):974−981.
[24] 聂小英,朱春晓,郑东升,陈阳峰,李自强,肖深根. 遮光处理对草珊瑚光合特性及叶片解剖结构的影响[J]. 西北植物学报,2021,41(6):995−1002. Nie XY,Zhu CX,Zheng DS,Chen YF,Li ZQ,Xiao SG. Effects of shading treatment on photosynthetic characteristics and leaf anatomical structure of Sarcandra glabra[J]. Acta Botanica Boreali-Occidentalia Sinica,2021,41(6):995−1002.
[25] 陈德兴,王天铎. 叶片叶肉结构对环境光强的适应及对光合作用的影响[J]. 应用生态学报,1990,1(2):142−148. Chen DX,Wang TD. Adaptation of leaf mesophyll structure to environmental light condition and its effect on leaf photosynthesis[J]. Chinese Journal of Applied Ecology,1990,1(2):142−148.
[26] 孙小玲,许岳飞,马鲁沂,周禾. 植株叶片的光合色素构成对遮阴的响应[J]. 植物生态学报,2010,34(8):989−999. Sun XL,Xu YF,Ma LY,Zhou H. A review of acclimation of photosynthetic pigment composition in plant leaves to shade environment[J]. Chinese Journal of Plant Ecology,2010,34(8):989−999.
[27] Lichtenthaler HK,Ač A,Marek MV,Kalina J,Urban O. Differences in pigment composition,photosynthetic rates and chlorophyll fluorescence images of sun and shade leaves of four tree species[J]. Plant Physiol Biochem,2007,45(8):577−588. doi: 10.1016/j.plaphy.2007.04.006
[28] 李焰焰,张紫薇,黄薇,聂传朋. 马缨丹光合色素及叶绿素荧光参数分析[J]. 生物学杂志,2022,39(2):29−33. Li YY,Zhang ZW,Huang W,Nie CP. Leaf structure and chlorophyll fluorescence of Lantana camara[J]. Journal of Biology,2022,39(2):29−33.
[29] Björkman O,Demmig B. Photon yield of O2 evolution and chlorophyll fluorescence characteristics at 77 K among vascular plants of diverse origins[J]. Planta,1987,170(4):489−504. doi: 10.1007/BF00402983
[30] 高丽楠. 九寨沟2种沉水植物叶绿素荧光特性比较[J]. 浙江农业学报,2017,29(6):951−958. Gao LN. Comparison of chlorophyll fluorescence characteristics between two submerged macrophytes in Jiuzhaigou National Nature Reserve[J]. Acta Agriculturae Zhejiangensis,2017,29(6):951−958.
[31] 周哲宇,徐超,胡策,王海湘,梁谢恩,等. 毛竹快速生长期的叶绿素荧光参数特征[J]. 浙江农林大学学报,2018,35(1):75−80. Zhou ZY,Xu C,Hu C,Wang HX,Liang XE,et al. Chlorophyll fluorescence characteristics of Phyllostachys edulis during its fast growth period[J]. Journal of Zhejiang A& F University,2018,35(1):75−80.
[32] 宋玉芝,蔡炜,秦伯强. 太湖常见浮叶植物和沉水植物的光合荧光特性比较[J]. 应用生态学报,2009,20(3):569−573. Song YZ,Cai W,Qin BQ. Photosynthetic fluorescence characteristics of floating-leaved and submersed macrophytes commonly found in Taihu Lake[J]. Chinese Journal of Applied Ecology,2009,20(3):569−573.
[33] 刘少华,陈国祥,杨艳华,王娜,施国新,吴国荣. 菱异形叶光合特性的比较[J]. 南京师大学报(自然科学版),2002,25(1):78−82. Liu SH,Chen GX,Yang YH,Wang N,Shi GX,Wu GR. A comparative study on photosynthetic activity of heteromorphous leaf from Trapa bispinosa R.[J]. Journal of Nanjing Normal University (Natural Science Edition),2002,25(1):78−82.
[34] Gao SJ,Chen SS,Li MQ. Rapid post-illumination oxygen consumption and its relation to photorespiration[J]. Acta Phytophysiologica Sinica,1988,14(4):313−317.
[35] 张依南,张蔚,田昆,孙梅,戴强,等. 不同水位下莼菜叶片气孔及光合特性的相关性分析[J]. 西南林业大学学报(自然科学),2019,39(5):35−42. Zhang YN,Zhang W,Tian K,Sun M,Dai Q,et al. Correlation analysis of stomatal and photosynthetic characteristics of Brasenia schreberi leaves under different water levels[J]. Journal of Southwest Forestry University (Natural Sciences),2019,39(5):35−42.
-
其他相关附件
-
PDF格式
厚富霞 附图1~附图4 点击下载(474KB)
-



 下载:
下载: